题目内容
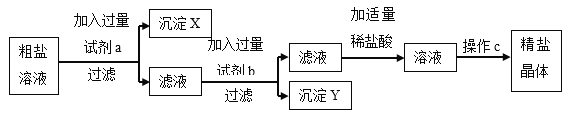
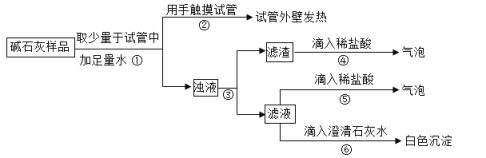
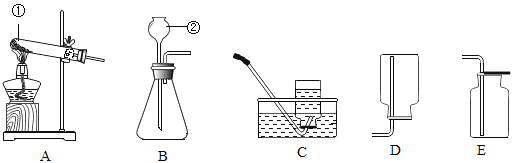
【题目】铁是日常生活中最常见的金属,据资料介绍:氧化铁在隔绝空气的条件下高温加热能生成黑色固体和一种气体。小明在实验室进行了下列实验:
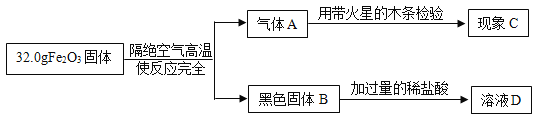
根据以上图示回答问题:
(1)气体A的化学式为_____,现象C是_____。
(2)对黑色固体B的探究:
(实验现象)在向黑色固体B中加过量稀盐酸的实验过程中,没有观察到有气泡产生。由此可知黑色固体B中没有铁,判断依据是_____(用化学方程式表示)
(查阅资料)①氧化亚铁和四氧化三铁都是黑色固体②它们都可以和稀盐酸或稀硫酸反应,其中四氧化三铁与盐酸反应的化学方程式为:Fe3O4+8HCl=2FeCl3+FeCl2+4H2O。
(猜想)黑色固体B是Ⅰ、FeO Ⅱ、Fe3O4 Ⅲ、_____。
(实验分析)
①小亮认为,如果猜想Ⅱ 成立,则溶液D中的溶质为_____;
②小意认为,要确定黑色固体B的组成,还应该继续称量B的质量。若实验称得黑色固体B的质量为30.4g,则B中铁、氧元素的质量比为_____,猜想_____成立。则氧化铁分解的化学方程式为_____
【答案】O2 带火星的木条复燃 Fe+2HCl═FeCl2+H2↑ FeO、Fe3O4 HCl、FeCl3、FeCl2 14:5 Ⅲ 4Fe2O3![]() 2FeO+2Fe3O4+O2↑
2FeO+2Fe3O4+O2↑
【解析】
(1)由质量守恒定律可知,氧化铁分解生成的气体是氧气,氧气的化学式为O2,现象C是带火星的木条复燃。
故填:O2;带火星的木条复燃。
(2)[实验现象]
在向黑色固体B中加过量稀盐酸的实验过程中,没有观察到有气泡产生。由此可知黑色固体B中没有铁,判断依据是铁能和稀盐酸反应生成氯化亚铁和氢气,反应的化学方程式为:Fe+2HCl═FeCl2+H2↑。
故填:Fe+2HCl═FeCl2+H2↑。
[猜想]
黑色固体B是Ⅰ、FeOⅡ、Fe3O4Ⅲ、FeO、Fe3O4。
故填:FeO、Fe3O4。
[实验分析]
①如果猜想Ⅱ成立,则溶液D中的溶质有过量稀盐酸中的氯化氢、四氧化三铁和稀盐酸反应生成的氯化铁和氯化亚铁。
故填:HCl、FeCl3、FeCl2。
②32.0g氧化铁中铁元素质量为:32.0g×![]() =22.4g,氧元素质量为:32.0g-22.4g=9.6g,
=22.4g,氧元素质量为:32.0g-22.4g=9.6g,
反应生成氧气质量为:32.0g-30.4g=1.6g,
黑色固体B中氧元素质量为:9.6g-1.6g=8g,
则B中铁、氧元素的质量比为:22.4g:8g=14:5,
氧化亚铁中铁元素、氧元素质量比为:56:16=7:2,四氧化三铁中铁元素、氧元素质量比为:168:64=21:8,
由以上数据可知,黑色固体B是氧化亚铁和四氧化三铁的混合物,即猜想Ⅲ成立;
则氧化铁分解生成氧化亚铁、四氧化三铁和氧气,反应的化学方程式为:4Fe2O3![]() 2FeO+2Fe3O4+O2↑。
2FeO+2Fe3O4+O2↑。
故填:14:5;Ⅲ;4Fe2O3![]() 2FeO+2Fe3O4+O2↑。
2FeO+2Fe3O4+O2↑。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】小明对铁的锈蚀进行如下探究,室温时,将包有样品的滤纸包用大头针固定在橡胶塞上,迅速塞紧,装置如图,观察到量筒内水沿导管慢慢进入广口瓶(净容积为146mL)。当温度恢复至室温,且量筒内水面高度不变时读数(此时瓶内氧气含量近似为零)。记录起始和最终量筒的读数以及所需时间如表。
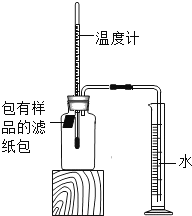
序号 | 样品 | 量筒起始 读数/mL | 量筒最终 读数/mL | 所需时间 /min |
1 | 1g铁粉、0.2g碳和10滴水 | 100 | 70 | 约120 |
2 | lg铁粉、0.2g碳、10滴水和少量NaCl | 100 | 70 | 约70 |
3 | …… | 100 | 70 | 约480 |
(1)实验①和②说明NaCl可以_____铁锈蚀的速率。
(2)实验开始后,广口瓶内温度有所上升,说明铁的锈蚀过程是_____(填“放热”或“吸热”)过程。
(3)实验结束后取出滤纸包,观察到有红棕色物质生成,该物质的化学式是_____。
(4)已知含碳能够加快铁的生锈速度,小明想通过实验①和③是探究碳对铁锈蚀速率的影响,请在表格空白处填写实验③的样品组成_____。
(5)该装置还可用于测量空气中氧气的含量,根据上述数据计算氧气的体积含量是_____(小数点后保留1位)。