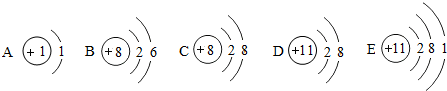题目内容
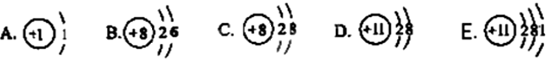
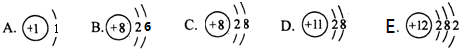
根据下列五种微粒的结构示意图,回答下列问题:

(1)图中微粒共能表示
(2)图中表示的阴离子是
(3)写出A2B2在一定条件下分解的化学方程式

(1)图中微粒共能表示
三
三
种元素,这几种元素共同组成化合物的化学式NaOH
NaOH
.(2)图中表示的阴离子是
C
C
(填字母).(3)写出A2B2在一定条件下分解的化学方程式
2H2O2
2H2O+O2↑
| ||
2H2O2
2H2O+O2↑
.
| ||
分析:(1)因为元素的种类由质子数决定,则五种微粒的结构示意图中,有几种质子数,便有几种元素;判断出元素种类,再组成化合物,利用化合价数值交叉法书写化学式;
(2)根据“阴离子中,核电荷数=质子数<核外电子数”,判断离子的情况.
(3)先判断出A2B2的化学式,再书写化学方程式;
(2)根据“阴离子中,核电荷数=质子数<核外电子数”,判断离子的情况.
(3)先判断出A2B2的化学式,再书写化学方程式;
解答:解:(1)因为元素的种类由质子数决定,则五种微粒的结构示意图中,有1、8、11三种质子数,则有三种元素;三种元素分别为氢元素、氧元素、钠元素,它们组成的化合物为氢氧化钠,已知钠元素的化合价为+1价,氢氧根为-1价,利用化合价数值交叉法书写化学式为NaOH;
(2)根据“阴离子中,核电荷数=质子数<核外电子数”,则判定C为阴离子;
(3)经判断,A为氢元素的原子,B为氧元素的原子,则A2B2为过氧化氢,故化学方程式为:2H2O2
2H2O+O2↑;
故答为:(1)三; NaOH;(2)C;(3)2H2O2
2H2O+O2↑;
(2)根据“阴离子中,核电荷数=质子数<核外电子数”,则判定C为阴离子;
(3)经判断,A为氢元素的原子,B为氧元素的原子,则A2B2为过氧化氢,故化学方程式为:2H2O2
| ||
故答为:(1)三; NaOH;(2)C;(3)2H2O2
| ||
点评:了解原子结构示意图与离子结构示意图的区别和联系;掌握元素的概念:具有相同核电荷数(核内质子数)的一类原子的总称;掌握正确书写化学方程式的方法步骤.

练习册系列答案
相关题目