题目内容
【题目】为了测定黄铜屑(由锌和铜形成的合金)样品的组成,甲、乙、丙、丁四位同学分别取样和稀硫酸反应(稀硫酸的密度为1.17g/cm3),实验数据记录如下表,请根据下表数据计算:
甲 | 乙 | 丙 | 丁 | |
取用黄铜屑的质量(g) | 8.0 | 8.0 | 8.0 | 12.0 |
取用稀硫酸的体积(mL) | 8.0 | 16.0 | 24.0 | 一定体积 |
残留金属的质量(g) | 6.7 | 5.4 | 4.8 | 8.1 |
(1)8 g黄铜屑中锌的质量为________g。
(2)丁同学所加稀硫酸的体积为________。
【答案】 3.2 24mL
【解析】(1)由实验甲可知,加入8.0mL稀硫酸时可消耗金属质量=8.0g-6.7g=1.3g;因此当加入24.0mL稀硫酸时,可消耗金属的质量=![]() ,而丙实验中样品质量减少=8.0g-4.8g=3.2g<3.9g,因此,丙实验样品中锌已完全反应,残留金属为铜,则8.0g黄铜屑中锌的质量为3.2g;(2)由实验甲可知,加入8.0mL稀硫酸时可消耗金属质量=8.0g-6.7g=1.3g;实验丁共消耗金属质量=12.0g-8.1g=3.9g,则所加入稀硫酸的体积=
,而丙实验中样品质量减少=8.0g-4.8g=3.2g<3.9g,因此,丙实验样品中锌已完全反应,残留金属为铜,则8.0g黄铜屑中锌的质量为3.2g;(2)由实验甲可知,加入8.0mL稀硫酸时可消耗金属质量=8.0g-6.7g=1.3g;实验丁共消耗金属质量=12.0g-8.1g=3.9g,则所加入稀硫酸的体积=![]() 。
。

练习册系列答案
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案
相关题目
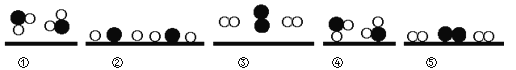
【题目】向100g水中不断加入固体A或改变温度,得到相应的溶液①~⑤。下列说法正确的是( )
![]()
资料:A的溶解度 | |||||
温度/℃ | 20 | 30 | 40 | 50 | 60 |
溶解度/g | 37.2 | 41.4 | 45.8 | 50.4 | 55.2 |
A. ②中A的质量分数最大 B. ③⑤中A的质量分数相等
C. ②④⑤的溶液为饱和溶液 D. ①③④⑤中没有固体存在