题目内容
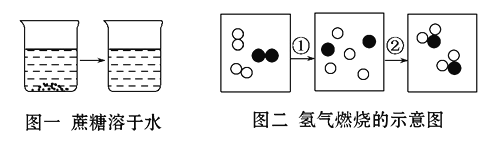
【题目】某海边化工厂利用海水中含有的氯化镁,经过一系列的化学反应,生成纯净的氯化镁,其主要生产过程如下:
![]()
石灰石(1)生石灰(2)熟石灰(3)氢氧化镁(4)氯化镁
请写出上述各步转化的化学方程式:
(1)_______________________________;
(2)_______________________________;
(3)_______________________________;
(4)__________________________________;
【答案】CaCO3![]() CaO+CO2↑CaO+H2O=Ca(OH)2Ca(OH)2+MgCl2=Mg(OH)2↓+CaCl2Mg(OH)2+2HCl=MgCl2+2H2O
CaO+CO2↑CaO+H2O=Ca(OH)2Ca(OH)2+MgCl2=Mg(OH)2↓+CaCl2Mg(OH)2+2HCl=MgCl2+2H2O
【解析】
(1)石灰石的主要成分是碳酸钙,碳酸钙在高温条件下反应生成氧化钙和二氧化碳,该反应的化学方程式为:CaCO3![]() CaO+CO2↑;(2)氧化钙与水反应生成氢氧化钙,该反应的化学方程式为:CaO+H2O=Ca(OH)2;(3)氢氧化钙与海水中的氯化镁反应生成氢氧化镁沉淀和氯化钙,该反应的化学方程式为:Ca(OH)2+MgCl2=Mg(OH)2↓+CaCl2;(4)氢氧化镁与盐酸反应生成氯化镁和水,该反应的化学方程式为:Mg(OH)2+2HCl=MgCl2+2H2O。
CaO+CO2↑;(2)氧化钙与水反应生成氢氧化钙,该反应的化学方程式为:CaO+H2O=Ca(OH)2;(3)氢氧化钙与海水中的氯化镁反应生成氢氧化镁沉淀和氯化钙,该反应的化学方程式为:Ca(OH)2+MgCl2=Mg(OH)2↓+CaCl2;(4)氢氧化镁与盐酸反应生成氯化镁和水,该反应的化学方程式为:Mg(OH)2+2HCl=MgCl2+2H2O。

【题目】请从A或B两题中任选一个作答,若两题均作答,按A计分。
A | B |
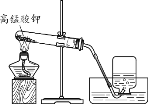
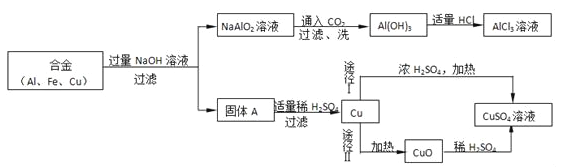
(1)电解水实验揭示了水的组成。下图实验中得到氧气的试管是_______(填“1”或“2”)。 (2)电解水的化学方程式为_________。
| (1)潜水时需要氧气,说明氧气能________。 (2)用高锰酸钾制取氧气的化学方程式为_________。
|
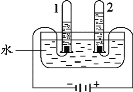
【题目】某实验小组做“滴水生火”实验,向包裹过氧化钠(Na2O2)的棉花上滴水,观察到棉花燃烧。
资料:Na2O2与H2O反应生成O2和NaOH
(实验1)验证反应的生成物
步骤 | 操作 | 现象 |
① | 取0.5 g Na2O2固体于锥形瓶中,加入50 mL蒸馏水,得溶液A | 固体全部消失,产生大量气泡 |
② | 将带火星的木条伸入锥形瓶 | _____ |
③ | 取5 mL溶液A于试管中,滴加1滴酚酞溶液 | 溶液变红 |
(1)证明②中有O2生成的现象是_____。
(2)依据③的现象,判断溶液A呈_____(填“酸性”、“碱性”或“中性”)。
(发现问题)③中溶液变红后,约2分钟褪为无色。
(查阅资料)(1)Na2O2与H2O反应分为两步:
①Na2O2与H2O反应生成H2O2和NaOH ②H2O2分解
(2)通常条件下,NaOH溶液与MnO2不反应
(3)H2O2有漂白性,能使变红的酚酞溶液褪色
(4)向5 mL 不同浓度的NaOH溶液中滴加1滴酚酞溶液,现象如下表:
NaOH溶液的浓度 | 30% | 10% | 1% |
现象 | 变红,15 s后褪色 | 变红,40 s后褪色 | 变红,10分钟内 不褪色 |
(猜想与假设)本实验中,溶液褪色的原因可能是:
a.生成的O2
b.溶液中的H2O2
c.溶液中NaOH的浓度
(实验2)验证猜想
编号 | 实验 |
I |
|
II | 取10 mL 溶液A于试管中,加入适量MnO2,将带火星的木条伸入试管。产生无色气体,带火星的木条复燃 |
III | i. 取10 mL 溶液A于试管中,……,过滤 |
ii. 取5 mL滤液于试管中,滴加1滴酚酞溶液。溶液变红,10分钟内不褪色 |
(实验结论)猜想a不成立,猜想b成立,猜想c不成立
综合以上信息,回答下列问题:
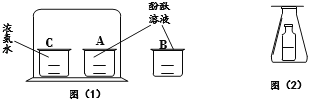
(3)实验I的现象是_____。
(4)实验II的目的是_____。产生无色气体的原因是_____(用化学方程式表示)。
(5)补全实验i:取10 mL 溶液A于试管中,_____,过滤。