题目内容
氧气和二氧化碳都是人类赖以生存的气体,因此研究其制法极为重要.
①工业上用分离液态空气的方法制取氧气,主要是利用了氧气和氮气的________不同.二氧化碳的工业制法与实验室制法不约而同地选择了碳酸钙(大理石或石灰石),不仅因为这种原料含有________(填“钙元素”或“碳酸根”),而且来源非常广泛.
②某小组根据实验室制取氧气的方法和思路研究二氧化碳的实验室制法.
【确定反应原理】
Ⅰ.实验室制取二氧化碳的反应原理是(写化学方程式)________.
Ⅱ.甲同学认为:应该选择反应C+O2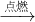 CO2制取二氧化碳,乙同学不同意甲的观点,乙同学的理由是(写一条)________.
CO2制取二氧化碳,乙同学不同意甲的观点,乙同学的理由是(写一条)________.
【确定实验装置】
Ⅰ.写出下列编号仪器的名称:③________;④________.
Ⅱ.若要制取一瓶二氧化碳气体所需仪器的编号为________.
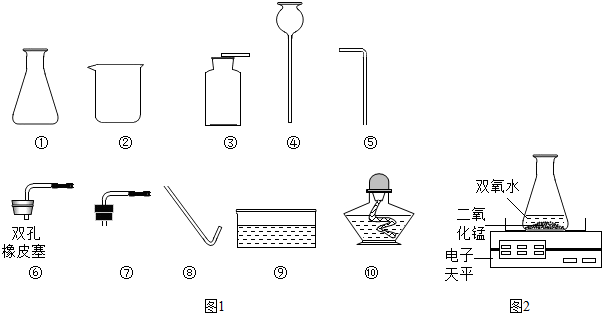
Ⅲ.实验室制取气体发生装置的选择依据是________,收集装置的选择依据是________.
A.反应物状态B.气体的密度C.反应的条件D.气体溶解性
【进行制取实验】
Ⅰ.验满二氧化碳气体的方法是________.
Ⅱ.写出检验二氧化碳气体的反应的化学方程式________.
③某同学利用双氧水分解的反应测定双氧水的浓度.他用图2装置进行实验.
Ⅰ.若该反应产生0.01mol氧气,则参加反应的过氧化氢的物质的量为________(列式计算).
Ⅱ.气体从溶液中逸出时会带出水蒸气,该因素将导致上述实验测定的双氧水的溶质质量分数________(填“偏大”或“偏小”).
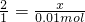 x=0.02mol 偏大
x=0.02mol 偏大分析:工业上用分离液态空气的方法制取氧气,主要是利用了氧气和氮气的沸点不同,二氧化碳的工业制法与实验室制法不约而同地选择了碳酸钙,是因为碳酸钙中有碳酸根,而且来源非常广泛,价格便宜;制取装置包括加热和不需加热两种,实验室制取CO2,是在常温下,用碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热,若要制取一瓶二氧化碳气体所需仪器有:锥形瓶、双孔橡皮塞、长颈漏斗、玻璃管、集气瓶、玻璃片等.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.甲同学认为:应该选择反应C+O2
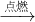 CO2制取二氧化碳,乙同学不同意甲的观点,乙同学的理由是:制得的气体不纯或不便于收集.集气瓶收集气体的仪器,长颈漏斗方便加液体药品;二氧化碳的验满方法是:将一根燃着的木条平放在集气瓶口,木条熄灭,证明满了;二氧化碳一般用澄清的石灰水检验:把气体通入澄清的石灰水中,石灰水变浑浊,就证明是二氧化碳.气体从溶液中逸出时会带出水蒸气,该因素将导致上述实验测定的双氧水的溶质质量分数偏大,因为氧气的质量偏大了.
CO2制取二氧化碳,乙同学不同意甲的观点,乙同学的理由是:制得的气体不纯或不便于收集.集气瓶收集气体的仪器,长颈漏斗方便加液体药品;二氧化碳的验满方法是:将一根燃着的木条平放在集气瓶口,木条熄灭,证明满了;二氧化碳一般用澄清的石灰水检验:把气体通入澄清的石灰水中,石灰水变浑浊,就证明是二氧化碳.气体从溶液中逸出时会带出水蒸气,该因素将导致上述实验测定的双氧水的溶质质量分数偏大,因为氧气的质量偏大了.解答:①工业上用分离液态空气的方法制取氧气,主要是利用了氧气和氮气的沸点不同,二氧化碳的工业制法与实验室制法不约而同地选择了碳酸钙,是因为碳酸钙中有碳酸根,而且来源非常广泛,价格便宜;故答案为:沸点 碳酸根
②【确定反应原理】碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,配平即可;甲同学认为:应该选择反应C+O2
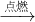 CO2制取二氧化碳,乙同学不同意甲的观点,乙同学的理由是:制得的气体不纯或不便于收集;故答案为:CaCO3+2HCl=CaCl2+H2O+CO2↑;制得的气体不纯或不便于收集
CO2制取二氧化碳,乙同学不同意甲的观点,乙同学的理由是:制得的气体不纯或不便于收集;故答案为:CaCO3+2HCl=CaCl2+H2O+CO2↑;制得的气体不纯或不便于收集【确定实验装置】集气瓶收集气体的仪器,长颈漏斗方便加液体药品,若要制取一瓶二氧化碳气体所需仪器有:锥形瓶、双孔橡皮塞、长颈漏斗、玻璃管、集气瓶、玻璃片等,气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关;故答案为:集气瓶;长颈漏斗;①③④⑤⑥;A、C; B、D
【进行制取实验】二氧化碳的验满方法是:将一根燃着的木条平放在集气瓶口,木条熄灭,证明满了;二氧化碳一般用澄清的石灰水检验:把气体通入澄清的石灰水中,石灰水变浑浊,就证明是二氧化碳;故答案为:燃着的木条放在集气瓶瓶口,木条火焰熄灭;CO2+Ca(OH)2=CaCO3↓+H2O
③Ⅰ、设参加反应的过氧化氢的物质的量为x
2H2O
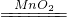 2H2O+O2↑
2H2O+O2↑2 1
x 0.01mol
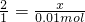 x=0.02mol
x=0.02mol答:参加反应的过氧化氢的物质的量为0.02mol.
Ⅱ、气体从溶液中逸出时会带出水蒸气,该因素将导致上述实验测定的双氧水的溶质质量分数偏大,因为氧气的质量偏大了,故答案为:偏大
点评:本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写和有关的计算,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关,有关的计算要准确.本考点是中考的重要考点之一,主要出现在实验题中.

小杰和小燕学习了碳单质的化学性质后,知道碳与氧气反应,若反应物的量不同,生成物不同。于是两人联想到木炭粉与氧化铜发生的反应可能有:
①C+2CuO 2Cu+CO2↑ ②C+CuO
2Cu+CO2↑ ②C+CuO Cu+CO↑
Cu+CO↑
他们想来验证自己的想法,请你和他们一起进行探究:(请完成下列空白处)
【提出问题】木碳与氧化铜反应除生成单质铜外,另一种生成物是什么?
【猜想与假设】木炭粉与氧化铜反应生成物有三种可能:
⑴产物是铜和一氧化碳 ⑵产物是铜和二氧化碳 ⑶产物是 ①▲ 。
【设计方案】
⑴检验CO2的方法是 ②▲ 。(用方程式表示)
⑵如何检验产物中是否存在CO,两位同学分别提出了检验CO的方案,但都被大家否定了。请在下表中写出不可行的原因。
检验方案 | 不可行的原因 | |
小杰 | 把小动物放在收集的气体中,观察能否存活 | ③▲ |
小燕 | 点燃生成的气体,观察能否燃烧 | ④▲ |
查阅资料后,他们把滤纸浸泡在磷钼酸与氯化钯的黄色混合液中,制成试纸(试纸遇一氧化碳立刻变蓝,而遇二氧化碳不反应)
【实验结论】设计的实验装置(如下图1):

实验现象 | 实验结论 |
A中固体由黑色变成红色 | 有Cu生成 |
B中黄色试纸变蓝 | 有 ⑤▲ 生成 |
C中 ⑥▲ | 有CO2生成 |
【反思与评价】
⑴如果A装置中的试管口高于试管底部,在实验过程中可能造成的后果是 ⑦▲ 。
⑵实验结束时,为防止铜被氧化,必须先停止加热,待铜冷却后再将试管口的橡皮塞取下,因此若没有B试剂瓶,可能导致的后果是 ⑧▲ 。
⑶根据实验结论,从环保的角度考虑,上述装置C后应添加的装置是 ⑨▲ 。
【拓展与交流】
如果用如图2装置代替图1中的A装置,这样既可以排尽试管中的空气,又能将反应产生的气体都“赶”出来,该气体可能是 ⑩▲ 。