题目内容
【题目】回答下列有关的实验问题:

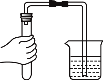
(1)实验一中,打开止水夹进入瓶中的水不足五分之一,其原因是______;
(2)实验二中,观察到的现象是___________;
(3)实验三电解水过程中,正、负两极产生气体的体积比约为_______;
(4)实验四中发生的反应用化学方程式表示为: Na2CO3+2HCl===2NaCl+H2O+CO2↑。若用其验证质量守恒定律不能得到正确结论,在不更换药品的情况下改进,使其遵守质量守恒定律,你的改进方法是_______。
【答案】红磷量不足(或装置气密性不好、未等装置冷却到室温就打开止水夹) 甲中酚酞溶液变红 1:2 将烧杯换成锥形瓶,并塞上胶塞,套上气球(或将装置改成密封装置等合理即可)
【解析】
(1)实验一中,打开止水夹进入瓶中的水不足五分之一,其原因可能是红磷量不足或装置气密性不好或未等装置冷却到室温就打开止水夹;
(2)实验二中,浓氨水具有挥发性,且氨水显碱性,能使酚酞溶液变红,故观察到的现象是甲中酚酞溶液变红;
(3)电解水过程中,正极产生氧气,负极产生氢气,正、负两极产生气体的体积比约为1:2;
(4)该反应生成了气体二氧化碳,有气体逸出,故用其验证质量守恒定律不能得到正确结论,在不更换药品的情况下,可以将烧杯换成锥形瓶,并塞上胶塞或套上气球或将装置改成密封装置等。

 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案【题目】某化学兴趣小组同学在整理实验室药品时发现一瓶未盖好盖子的氢氧化钠固体,为了探究此氧氢氧化钠固体是否变质,同学们进行了有关实验.请你与他们一起完成以下探究活动:
(知识回顾)氢氧化钠变质的化学方程式为______________.
(假设猜想)假设一:氧氧化钠没有变质 假设二:氢氧化钠变质了
(实验探究)同学们设计了多种方法进行验证.
操作 | 现象 | 结论 | |
方法一 | 取该样品少量于试管里,加入适量的水,振荡,样品全部溶于水,再向其中滴加酚酞试液 | 溶液变红色 | 样品变质了 |
方法二 | 取该样品少量于试管里,加入足量稀盐酸 | 有气泡产生 | 样品变质了 |
方法三 | 取该样口少量于试管里,加入适量的水,振荡,样品全部溶于水,再加入足量的氯化钙溶液 | 溶液变浑浊 | 样品变质了 |
(得出结论)氢氧化钠变质了
(讨论交流)经过讨论,同学们一致认为只有方法____________的探究过程是严密的.另外两种方法探究过程出错的原因是____________(任选一种方法进行解释).
(拓展迁移)
(1)同学们继续研究氢氧化钠固体是部分变质还是全部变质,过程如下:

A溶液中的溶质为___________;现象B是__________.
(2)为了将部分变质的氢氧化钠固体中的杂质除去,同学们做了如下实验:取固体加水溶解,向溶液中加入适量的_____________溶液,过滤后蒸发,即可得到纯净的氢氧化钠固体.
【题目】下图所示为实验室中常见的气体制备和收集装置。
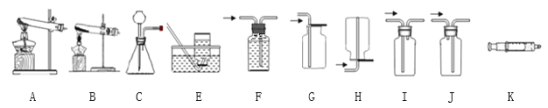
(1)实验室用高锰酸钾制取氧气,应选用发生装置_________(填字母序号,下空相同),收集装置可以选择__________,反应的文字表达为_______。
(2)注射器K可用于检查装置C的气密性,步骤如下:
①向锥形瓶中加入水至___________处。
②将注射器K连接到装置C的导管口处。
③缓慢拉动注射器K的活塞,观察到_______,表示装置C的气密性良好。
(3)为了研究用向上排空气法和排水法收集的氧气浓度是否有差异,做了如下实验:加热高锰酸钾固体,分别用两种方法各收集三瓶氧气,并使用传感器测定收集到的氧气浓度,数据见表。
收集方法 | 向上排空气法 | 排水法 | ||||
氧气浓度% | 79.6 | 79.7 | 79.9 | 90.0 | 89.8 | 89.3 |
氧气平均浓度% | 79.7 | 89.7 | ||||
①用向上排空气法收集氧气时,以__________为氧气集满标准;
用排水法收集氧气时,以观察到_________为氧气集满的标准。
②以上两种方法中,______________法收集到的氧气更纯净。
③向上排空气法收集到的氧气浓度只有80%左右的原因有_________。
A.氧气的密度略大于空气的密度
B.加热高锰酸钾固体产生氧气的浓度只有80%左右
C.当观察到带火星木条复燃时,集气瓶内还有空气
D.当氧气进入集气瓶时,瓶内空气与进入的氧气相互扩散
【题目】向烧杯中逐滴加入X溶液至过量(图甲),生成沉淀或气体的质量(纵坐标)与加入X溶液的质量(横坐标)关系符合图乙的是( )
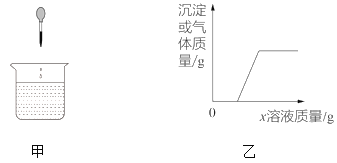
烧杯中的物质 | X溶液 | |
A | 氢氧化钠和硫酸钠溶液 | 氯化铁溶液 |
B | 稀硫酸和硫酸铜溶液 | 氢氧化钠溶液 |
C | 氯化钙和氯化钡溶液 | 碳酸钠溶液 |
D | 碳酸氢钠和氯化钠溶液 | 稀盐酸 |
A. A B. B C. C D. D