题目内容
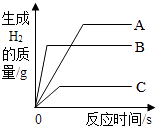
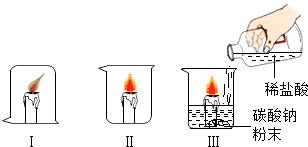
【题目】如图为某学习小组探究金属化学性质时所做的四个实验,仔细分析后回答下列问题:
(1)描述B中的实验现象 .
(2)写出C中反应的化学方程式 , 并指明反应类型: .
(3)要证明Cu、Fe、Ag的活动性顺序,至少要做的实验是(填序号).
(4)开始反应后D中溶液逐渐变为黄色,可能的原因是 .
【答案】
(1)铁丝表面附着了一层红色固体
(2)Zn+2HCl═ZnCl2+H2↑;置换反应
(3)AB
(4)铁钉表面有铁锈
【解析】解:(1)B中的实验现象是:铁丝表面附着了一层红色固体.
故填:铁丝表面附着了一层红色固体.(2)C中锌和稀盐酸反应的化学方程式为:Zn+2HCl═ZnCl2+H2↑,属于置换反应.故填:Zn+2HCl═ZnCl2+H2↑;置换反应.(3)要证明Cu、Fe、Ag的活动性顺序,至少要做的实验是AB,通过A证明铜比银活泼,通过B证明铁比铜活泼.故填:AB.(4)开始反应后D中溶液逐渐变为黄色,可能的原因是铁钉表面有铁锈,和稀硫酸反应生成了硫酸铁溶液.故填:铁钉表面有铁锈.
【考点精析】掌握金属材料的选择依据和书写化学方程式、文字表达式、电离方程式是解答本题的根本,需要知道黑色金属:通常指铁、锰、铬及它们的合金.重金属:如铜、锌、铅等;有色金属轻金属:如钠、镁、铝等;有色金属:通常是指除黑色金属以外的其他金属;注意:a、配平 b、条件 c、箭号.

 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案【题目】鉴别下列各组物质的方法不正确的是( )
选项 | 鉴别的物质 | 鉴别的方法 |
A | 纯水和矿泉水 | 观察是否澄清 |
B | 二氧化碳和一氧化碳 | 点燃,观察是否能燃烧 |
C | 水和过氧化氢溶液 | 加二氧化锰,观察是否有气泡 |
D | 冰和干冰 | 室温(20℃)放置,过一段时间观察是否有液体出现 |
A.A
B.B
C.C
D.D
【题目】设计对比实验,控制变量是学习化学的重要方法,下列对比实验不能达到目的是( )
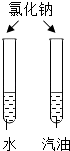
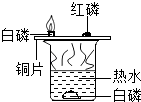
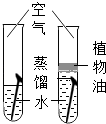
编号 | A | B | C | D |
实验设计 |
|
|
|
|
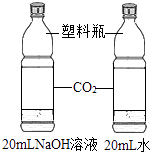
实验目的 | 探究同种物质在不同溶剂中的溶解性 | 探究物质燃烧的条件 | 探究铁生锈的条件 | 探究CO2与NaOH溶液能否发生反应 |
A.A
B.B
C.C
D.D