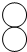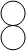题目内容
 工业上用甲和乙反应制备燃料丙.根据下列微观示意图得出的结论中,正确的是
工业上用甲和乙反应制备燃料丙.根据下列微观示意图得出的结论中,正确的是
- A.甲的化学式为CH2,每个甲的分子含有三个原子
- B.反应中甲、乙、丙的分子个数比为2:1:1
- C.乙、丙都是氧化物
- D.丙中C、H、O元素的质量比为12:3:8
D
分析:由三种物质的分子微观示意图判断分子构成,根据分子构成写出物质的化学式:甲物质的化学式为C2H4、乙物质的化学式为H2O、丙物质的化学式为C2H6O,利用三种物质的化学式完成对所得结论的评价.
解答:A、根据甲物质的分子微观示意图可知,该物质的化学式为C2H4;故结论A不正确;
B、根据三种物质的分子微观示意图可知,用甲和乙反应制备丙的化学方程式为C2H4+H2O═C2H6O,反应中甲、乙、丙的分子个数比为1:1:1;故结论B不正确;
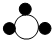
C、依据氧化物是含有氧元素的由两种元素组成的化合物,而根据乙物质的化学式为H2O可知它是氧化物,丙物质的化学式为C2H6O,共含有三种元素所以不是氧化物;故结论C不正确;
D、根据丙物质的分子微观示意图可知,该物质的化学式为C2H6O,则该物质中C、H、O元素的质量比为(12×2):(1×6):16=12:3:8;故结论D正确;
故选D.
点评:解答本题的关键由分子微观示意图确定分子构成,利用分子构成写出物质的化学式,重点考查了相关知识的运用能力.
分析:由三种物质的分子微观示意图判断分子构成,根据分子构成写出物质的化学式:甲物质的化学式为C2H4、乙物质的化学式为H2O、丙物质的化学式为C2H6O,利用三种物质的化学式完成对所得结论的评价.
解答:A、根据甲物质的分子微观示意图可知,该物质的化学式为C2H4;故结论A不正确;
B、根据三种物质的分子微观示意图可知,用甲和乙反应制备丙的化学方程式为C2H4+H2O═C2H6O,反应中甲、乙、丙的分子个数比为1:1:1;故结论B不正确;
C、依据氧化物是含有氧元素的由两种元素组成的化合物,而根据乙物质的化学式为H2O可知它是氧化物,丙物质的化学式为C2H6O,共含有三种元素所以不是氧化物;故结论C不正确;
D、根据丙物质的分子微观示意图可知,该物质的化学式为C2H6O,则该物质中C、H、O元素的质量比为(12×2):(1×6):16=12:3:8;故结论D正确;
故选D.
点评:解答本题的关键由分子微观示意图确定分子构成,利用分子构成写出物质的化学式,重点考查了相关知识的运用能力.

练习册系列答案
相关题目
(8分)物质丙是重要的化工产品,在国民经济中占有重要地位。工业上用甲和乙在高温高压加催化剂的条件下合成丙。甲、乙、丙的微观示意图见下表。
| 物质 | 甲 | 乙 | 丙 |  |
| 微观示意图 |  | 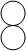 |  |
(2)甲、乙、丙中属于化合物的是(填序号) 。
(3)已知物质丙中氢元素的化合价为+1,则另一种元素的化合价为 。
(4)写出甲和乙合成丙反应的化学方程式 。
(5)现用10g的甲和60g的乙混合反应制取丙,反应一段时间后,经测定剩余甲的质量为4g,则剩余乙的质量为 g。
(6)在生产丙的原料中,甲是用水与碳高温反应(将水蒸汽通过高温碳层,这种方法又称为水煤汽法)制得的,这个过程还生成另一种产物一氧化碳;请你根据信息写出该反应的化学方程式 。
(8分)物质丙是重要的化工产品,在国民经济中占有重要地位。工业上用甲和乙在高温高压加催化剂的条件下合成丙。甲、乙、丙的微观示意图见下表。
|
物质 |
甲 |
乙 |
丙 |
|
|
微观示意图 |
|
|
|
(1)甲、乙、丙三种物质都是由(填“分子”、“原子”或“离子”) 构成的。
(2)甲、乙、丙中属于化合物的是(填序号) 。
(3)已知物质丙中氢元素的化合价为+1,则另一种元素的化合价为 。
(4)写出甲和乙合成丙反应的化学方程式 。
(5)现用10g的甲和60g的乙混合反应制取丙,反应一段时间后,经测定剩余甲的质量为4g,则剩余乙的质量为 g。
(6)在生产丙的原料中,甲是用水与碳高温反应(将水蒸汽通过高温碳层,这种方法又称为水煤汽法)制得的,这个过程还生成另一种产物一氧化碳;请你根据信息写出该反应的化学方程式 。
物质丙是重要的化工产品,在国民经济中占有重要地位.工业上用甲和乙在高温高压加催化剂的条件下合成丙.甲、乙、丙的微观示意图见下表.
| 物质 | 甲 | 乙 | 丙 | -----氮原子-----氢原子 |
| 微观示意图 |  | 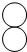 | 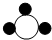 |
(2)甲、乙、丙中属于化合物的是(填序号)________.
(3)已知物质丙中氢元素的化合价为+1价,则另一种元素的化合价为________价.
(4)写出甲和乙合成丙反应的化学方程式________.
(5)现用10g的甲和60g的乙混合反应制取丙,反应一段时间后,经测定剩余甲的质量为4g,则剩余乙的质量为________g.
(6)在生产丙的原料中,甲是用水与碳高温反应(将水蒸汽通过高温碳层,这种方法又称为水煤汽法)制得的,这个过程还生成另一种产物一氧化碳;请你根据信息写出该反应的化学方程式________.