��Ŀ����
����Ŀ��ij��ȤС���ͬѧΪ̽�������Ļ�ԡ��Լ�ͭ��ʴ����������������ϵ��ʵ�飬��ϸ������ش��������⣺
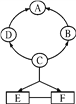
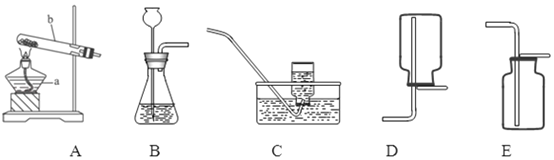
��1��ʵ��һ��С������ͼ1��ʾ������������������ݵĿ�����Ϊ�����ж�п���������Ļ��ǿ������ͬѧ��Ϊ����������������___________������ϡ����սӴ�ʱ������һ��ʱ�����ң�����ϡ����սӴ�ʱ��������ԭ�������___________��
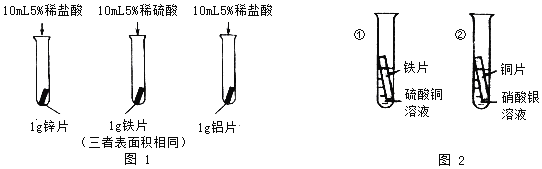
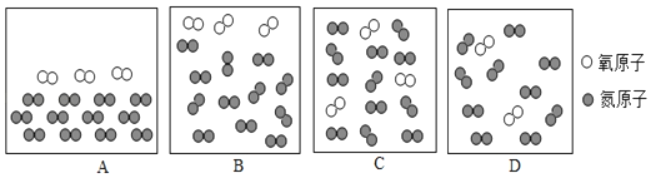
��2��ʵ�����Ϊ̽������ͭ�������ֽ�����Ե�˳��С���������ͼ2��������ʵ�飬����֤�����ֽ������˳������Ϊ�䷽��������___________����������������������������
a���Թܢ���������___________��
b���Թܢ��з�����Ӧ�Ļ�ѧ����ʽΪ___________��
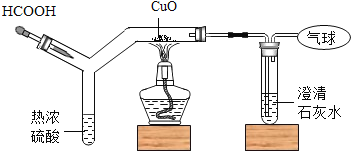
��3��ʵ������С����С����λͬѧ����ͭ���۾����ϳ�����һЩ��ɫ�����ա����������ϵ�֪��ͭ��Ļ�ѧ�ɷ��Ǽ�ʽ̼��ͭCu2��OH��2CO3���������ո��������̽�������������ʵ�飨ͼ3��ʾ������ش�
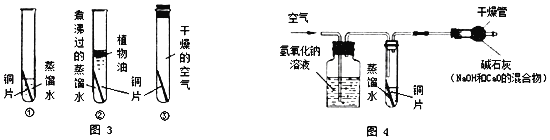
a���Ʋ�һ��ʱ�������ͭ�����___________�Թ��ڵ�ͭƬ������������������������������
b��С��ͬѧ��ΪҪŪ�嵼��ͭ��ʴ�����أ���Ӧ�ò���ʵ�飬����ͼ4��ʾ��ʵ�飬��Ŀ����___________��
���𰸡����õ��ͬ�� ��������������Ⱥ�ϡ���ᷴӦ�����Ȼ�����ˮ ���У� ��Ƭ����������ɫ���壻 Cu+2AgNO3��Cu��NO3��2+2Ag �� ̽��ͭ�����Ƿ�Ͷ�����̼�й�
��������
��1����ͬѧ��Ϊ�������������������õ��ͬ��
����ϡ����սӴ�ʱ��������ԭ���������������������Ⱥ�ϡ���ᷴӦ�����Ȼ�����ˮ��
������õ��ͬ����������������Ⱥ�ϡ���ᷴӦ�����Ȼ�����ˮ��
��2������ͼ2��������ʵ�飬����֤�����ֽ������˳��������Ϊ��Ƭ����������ɫ���壬����Ϊ��������ͭ��Ӧ��������������ͭ��˵������ͭ���ã�ͭƬ������������ɫ���壬����Ϊͭ����������Ӧ��������ͭ������˵��ͭ�������ã�
a���Թܢ�����������Ƭ����������ɫ���壻
b���Թܢ��з�����Ӧ�Ļ�ѧ����ʽΪ��Cu+2AgNO3��Cu��NO3��2+2Ag��
������У���Ƭ����������ɫ���壻Cu+2AgNO3��Cu��NO3��2+2Ag��
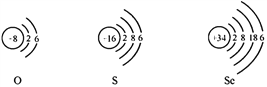
��3��a���Ʋ�һ��ʱ�������ͭ����Ǣ��Թ��ڵ�ͭƬ��������Ϊ��ʽ̼��ͭ�к���ͭԪ�ء���Ԫ�ء���Ԫ�غ�ͭԪ�أ�����ͭ����Ԫ�ء���Ԫ�ء�ͭԪ�ؽӴ�������ͭ����Ԫ�ء���Ԫ�ؽӴ�������ͭ����Ԫ�ء�ͭԪ�ؽӴ���
����١�
b����ͼ4��ʾ��ʵ�飬����������Һ�ܹ����տ����еĶ�����̼����Ŀ����̽��ͭ�����Ƿ�Ͷ�����̼�йء�
���̽��ͭ�����Ƿ�Ͷ�����̼�йء�

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�