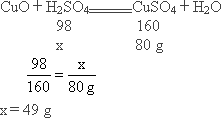题目内容
实验是进行科学探究的重要途径,在探究过程中,很多因素都会对实验结果产生影响.
(1)反应物的浓度不同,反应现象不同.请举出实例说明.
__________________________
(2)碳在充足的氧气中燃烧生成二氧化碳,在不足的氧气中燃烧生成一氧化碳.对比这两个反应可以得到的结论是________.
(3)H2在加热条件下可以与CuO反应,生成Cu和H2O.
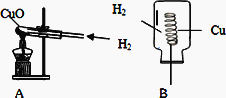
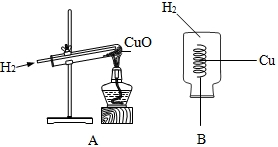
①亮亮同学利用图A装置完成了该实验.
实验步骤:先通入H2,再加热,实验结束后,先撤酒精灯,继续通入H2直至试管冷却.可观察到黑色CuO变成红色.
②明明同学利用右图B装置也完成了该实验.实验步骤:将铜丝在酒精灯外焰上加热变黑后,迅速伸入盛有H2的集气瓶中,片刻可观察到黑色CuO变为红色.
对比A、B两套装置,B装置的优点是________.
③在明明同学的实验中,当铜丝表明生成CuO后,若继续在酒精灯外焰上加热至炽热状态时,则与H2反应较快;若只加热至红热状态时,则反应较慢,甚至没有明现现象.对比这两种情况,可得到的结论是________.
(4)在用废铜屑制取硫酸铜的实验中,有下列两种方案可供选择:
甲方案:Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
乙方案:2CuO+O2![]() 2CuO
2CuO
CuO+H2SO4![]() CuSO4+2H2O
CuSO4+2H2O
①分别用上述两种方案制取80 g硫酸铜,甲方案参加反应的硫酸的质量为98 g,请计算乙方案中参加反应的硫酸的质量为多少?
②通过对比这两种实验方案及计算结果,你认为选用哪种方案更好?________;请说明你的理由________.
(5)通过对上述实验的对比与分析可知,探究某一化学问题时,除了应根据具体情况考虑恰当的实验装置外,还应考虑________等因素.
解析:
|
(1)硫在氧气里燃烧产生淡蓝色火焰,在氧气里燃烧产生蓝紫色火焰等(1分) (2)反应物的量不同,得到的生成物可能不同;或由量变可以引起质变等(1分) (3)②装置简单、操作简便、节约原料、节省时间等回答出一种即可(1分) ③温度越高,反应越快;或内因是变化的根据,外因是变化的条件等(1分) (4)①答:乙方案参加反应的硫酸的质量为49 g. 解:设乙方案参加反应的硫酸的质量为x. ②乙方案(1分) 此方案既可节省原料又可避免产生SO2污染空气(1分) (5)反应条件、反应物的用量、操作步骤等答出一条即可(1分) |

 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案