题目内容
某同学从定量角度研究双氧水制取氧气的过程,在原实验基础上增加了称量操作,具体做法是:取10%的双氧水和少量的二氧化锰放入气体发生装置,并对反应前后混合物的质量进行称量,记录如下:
| 反应过程 | 反应前 | 反应后 |
| 质量变化(不含容器质量) | 34.3g | 32.7g |
- A.二氧化锰的质量为0.3g
- B.最多得到氧气的质量为1.6g
- C.双氧水中过氧化氢的质量为3.4g
- D.反应后容器中水的质量为1.8g
D
分析:根据制取氧气的质量进行分析,反应物的浓度影响化学反应的速率,反应物的浓度越大,反应越剧烈,根据物质的质量差可以求得氧气的质量,根据反应的化学方程式可以确定生成的水和氧气的质量比,以及过氧化氢的质量,从而求得二氧化锰的质量.
解答:生成氧气的质量为:34.3g-32.7g=1.6g
设生成1.6g氧气需要过氧化氢的质量为x
2H2O2 2H2O+O2↑
2H2O+O2↑
68 32
x 1.6g
根据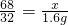 解得x=3.4g
解得x=3.4g
A、过氧化氢溶液的质量为:3.4g÷10%=34g,二氧化锰的质量为:34.3g-34g=0.3g,故A说法正确;
B、根据质量守恒定律,反应前物质的质量总和等于反应后物质的质量总和,生成氧气的质量为:34.3g-32.7g=1.6g,故B说法正确;
C、由上面的计算可知双氧水中过氧化氢的质量为3.4g,故C说法正确,
D、反应后容器中水的质量为:32.7g-0.3g=32.4g,故D说法错误.
故选D.
点评:本题考查了实验室制取氧气的反应原理以及根据化学方程式和溶质质量分数的计算,完成此题,可以依据已有的知识结合题干提供的信息进行.
分析:根据制取氧气的质量进行分析,反应物的浓度影响化学反应的速率,反应物的浓度越大,反应越剧烈,根据物质的质量差可以求得氧气的质量,根据反应的化学方程式可以确定生成的水和氧气的质量比,以及过氧化氢的质量,从而求得二氧化锰的质量.
解答:生成氧气的质量为:34.3g-32.7g=1.6g
设生成1.6g氧气需要过氧化氢的质量为x
2H2O2
 2H2O+O2↑
2H2O+O2↑68 32
x 1.6g
根据
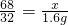 解得x=3.4g
解得x=3.4gA、过氧化氢溶液的质量为:3.4g÷10%=34g,二氧化锰的质量为:34.3g-34g=0.3g,故A说法正确;
B、根据质量守恒定律,反应前物质的质量总和等于反应后物质的质量总和,生成氧气的质量为:34.3g-32.7g=1.6g,故B说法正确;
C、由上面的计算可知双氧水中过氧化氢的质量为3.4g,故C说法正确,
D、反应后容器中水的质量为:32.7g-0.3g=32.4g,故D说法错误.
故选D.
点评:本题考查了实验室制取氧气的反应原理以及根据化学方程式和溶质质量分数的计算,完成此题,可以依据已有的知识结合题干提供的信息进行.

练习册系列答案
相关题目
(2012?济宁)某同学从定量角度研究双氧水制取氧气的过程,对原实验进行部分改进,增加了称量操作.具体做法是:取10%的双氧水和少量的二氧化锰放入气体发生装置,并对反应前后混合物的质量进行称量,记录如下:
|
(2013?朝阳区二模)某同学从定量角度研究双氧水制取氧气的过程,在原实验基础上增加了称量操作,具体做法是:取10%的双氧水和少量的二氧化锰放入气体发生装置,并对反应前后混合物的质量进行称量,记录如下:
|
某同学从定量角度研究氯酸钾制取氧气的过程,对原实验进行部分改进,增加了称量煤作.具体做法是:取一定量氯酸钾和少量的二氧化锰放入气体发生装置,并对反应前后混合物的质量进行称量,记录如下:
|
某同学从定量角度研究双氧水制取氧气的过程,在原实验基础上增加了称量操作,具体做法是:取10%的双氧水和少量的二氧化锰放入气体发生装置,并对反应前后混合物的质量进行称量,记录如下:
|
反应过程 |
反应前 |
反应后 |
|
质量变化(不含容器质量) |
34.3g |
32.7g |
若反应后,双氧水分解完全且氧气全部逸出,下列结论不正确的是( )
A.二氧化锰的质量为0.3g
B.最多得到氧气的质量为1.6g
C.双氧水中过氧化氢的质量为3.4g
D.反应后容器中水的质量为1.8g