��Ŀ����
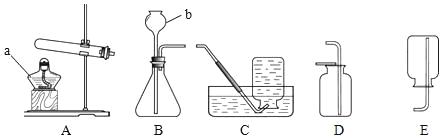
����Ŀ������ͬѧҪ̽��þ��ȼ��ǰ�������ı仯����������������Ҫʹ�õ���______���پƾ��Ƣ�����̨������ǯ��ɰֽ���ԹܼТ�������ƽ![]() �����
�����![]() ����ʯ�����Ϸ���ȼþ�����÷�Ӧ�Ļ�ѧ����ʽΪ______��ϸ�ĵ�����ͬѧ����������������������ɫ�������ɡ�ͬѧ������ʦָ���½���������ʵ��̽����
����ʯ�����Ϸ���ȼþ�����÷�Ӧ�Ļ�ѧ����ʽΪ______��ϸ�ĵ�����ͬѧ����������������������ɫ�������ɡ�ͬѧ������ʦָ���½���������ʵ��̽����
��������⣩______��
��ʵ��̽�������õ���ɫ����Ͷ�뵽ʢ��ˮ���ձ��С�
��ʵ���������ձ��в�����ɫ���������д̼��Եİ�ζ���������
����ʦָ����������Ӧ�����İ�ɫ����Ϊ![]() �����ɵ�����Ϊ
�����ɵ�����Ϊ![]() ���˷�Ӧ������û���κ�Ԫ�صĻ��ϼ۷����ı䡣
���˷�Ӧ������û���κ�Ԫ�صĻ��ϼ۷����ı䡣
�����サ�������˵���ɫ�������ʽ�������Ԫ����ɣ���������ˮ��Ӧ�Ļ�ѧ����ʽΪ______�����ɵ���ɫ�����ԭ����______��
���𰸡��٢ۢܣ� 2Mg +O2![]() 2MgO �õ���ɫ�����ǵ���þ�� Mg3N2+6H2O=3Mg(OH)2��+2NH3�� �����еĵ�����þ�����˷�Ӧ
2MgO �õ���ɫ�����ǵ���þ�� Mg3N2+6H2O=3Mg(OH)2��+2NH3�� �����еĵ�����þ�����˷�Ӧ
��������
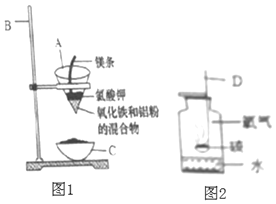
þȼ��ʵ����Ҫ��ɰֽ��ĥþ������ȥþ�������������þƾ��Ƶ�ȼþ��������Ҫ������ǯ�г֣�����Ҫ����������٢ۢܣ�þ�������ڵ�ȼ����������������þ������ʽ����2Mg +O2![]() 2MgO��
2MgO��
[�������]
�����к����϶���ǵ������õ���ɫ��������ǵ�����þ��Ӧ�õ��ģ�����õ���ɫ�����ǵ���þ��
[���サ��]
���˵���ɫ�������ʽ�������Ԫ����ɣ���ô����þ��ˮ��Ӧ����������þ�Ͱ�������ƽ���ɣ�����ʽ����Mg3N2+6H2O=3Mg(OH)2��+2NH3�������ɵ���ɫ�����ԭ���ǿ����еĵ�����þ�����˷�Ӧ����������еĵ�����þ�����˷�Ӧ��

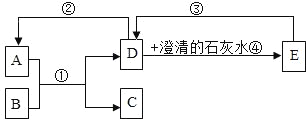
����Ŀ������ʵ�鷽��һ���ܴﵽʵ��Ŀ����![]() ����
����![]()
ѡ�� | ʵ��Ŀ�� | ʵ�鷽�� |
A | ����һƿ�����Ƿ�Ϊ | ��ȼ�ŵ�ľ������ƿ�� |
B | ���� | �ֱ��ȼ���ڻ����Ϸ���һ�����ձ� |
C | ��ȥ | ͨ�����ȵ�CuO |
D | ��ȥKCl�е����� | ���� |
A. A B. B C. C D. D