题目内容
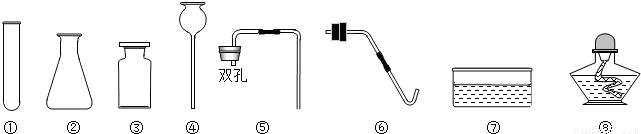
(2009?香坊区一模)小明的父亲买回一些钾肥,其包装袋上的部分内容如图所示,为确定该化肥的纯度是否符合标准,小明同学取10g化肥样品加入50g某盐酸盐溶液恰好完全反应后,过滤、洗涤、烘干得沉淀的质量为11.65g| 名称:硫酸钾 化学式:K2SO4 纯度:95% ×××化肥厂 |
(2)发生反应的化学方程式______;
(3)10g该化肥中K2S04的质量为______;
(4)通过计算该化肥的纯度是否符合包装袋上的说明______;
(5)所用盐酸盐溶液中溶质的质量分数______;
(6)恰好完全反应时所得溶液中溶质的质量分数______.
【答案】分析:本题要测定硫酸钾的质量,由于其可溶于水,因此一般将其转化为可称量质量的沉淀,一般选用含钡离子的氯化钡(硝酸钡)溶液与硫酸钾生成的硫酸钡沉淀,然后进行过滤分离、提纯和干燥等操作,根据称量得到硫酸钡的质量计算出硫酸钾的质量、氯化钾的质量以及盐酸盐的溶质质量分数等相关数据.最后求出硫酸钾固体在样品中的质量分数以及氯化钾溶液的溶质质量分数.
解答:解:(1)选用氯化钡与硫酸钾生成的硫酸钡沉淀,故答案为BaCl2
(2)根据复分解反应的特点进行书写即可:BaCl2+K2SO4═BaSO4↓+2KCl(注意沉淀符号)
(3)和(5)设10g该化肥中K2S04的质量为X;所用氯化钡溶液的溶质质量分数为Y;生成的氯化钾的质量为Z;
BaCl2+K2SO4═BaSO4↓+2KCl
208 174 233 149
50g×Y X 11.65g Z
列比例求出X=8.7g Y=20.8% Z=7.45g
(4)K2S04的质量分数为: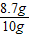 ×100%=87%<95%不合格
×100%=87%<95%不合格
(6)KCl溶液的溶质质量分数为: ×100%=15.4%
×100%=15.4%
答::(1)BaCl2(2)BaCl2+K2SO4═BaSO4↓+2KCl(3)8.7g(4)否(5)20.8%(6)15.4%
点评:本题主要是利用硫酸根离子与钡离子反应生成沉淀,然后进行分离操作可得称得硫酸钡的质量,进行分析求出其它相关数据.要求出两个数据:一是生成的氯化钾的质量;二是正确表示出溶液的质量.在表示溶液质量时必须将生成的沉淀排除在溶液外,有些反应生成气体也得一并减去.
解答:解:(1)选用氯化钡与硫酸钾生成的硫酸钡沉淀,故答案为BaCl2
(2)根据复分解反应的特点进行书写即可:BaCl2+K2SO4═BaSO4↓+2KCl(注意沉淀符号)
(3)和(5)设10g该化肥中K2S04的质量为X;所用氯化钡溶液的溶质质量分数为Y;生成的氯化钾的质量为Z;
BaCl2+K2SO4═BaSO4↓+2KCl
208 174 233 149
50g×Y X 11.65g Z
列比例求出X=8.7g Y=20.8% Z=7.45g
(4)K2S04的质量分数为:
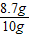 ×100%=87%<95%不合格
×100%=87%<95%不合格(6)KCl溶液的溶质质量分数为:
 ×100%=15.4%
×100%=15.4%答::(1)BaCl2(2)BaCl2+K2SO4═BaSO4↓+2KCl(3)8.7g(4)否(5)20.8%(6)15.4%
点评:本题主要是利用硫酸根离子与钡离子反应生成沉淀,然后进行分离操作可得称得硫酸钡的质量,进行分析求出其它相关数据.要求出两个数据:一是生成的氯化钾的质量;二是正确表示出溶液的质量.在表示溶液质量时必须将生成的沉淀排除在溶液外,有些反应生成气体也得一并减去.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
(2009?香坊区一模)小明的父亲买回一些钾肥,其包装袋上的部分内容如图所示,为确定该化肥的纯度是否符合标准,小明同学取10g化肥样品加入50g某盐酸盐溶液恰好完全反应后,过滤、洗涤、烘干得沉淀的质量为11.65g
(1)写出所加溶液中的溶质______;
(2)发生反应的化学方程式______;
(3)10g该化肥中K2S04的质量为______;
(4)通过计算该化肥的纯度是否符合包装袋上的说明______;
(5)所用盐酸盐溶液中溶质的质量分数______;
(6)恰好完全反应时所得溶液中溶质的质量分数______.
| 名称:硫酸钾 化学式:K2SO4 纯度:95% ×××化肥厂 |
(2)发生反应的化学方程式______;
(3)10g该化肥中K2S04的质量为______;
(4)通过计算该化肥的纯度是否符合包装袋上的说明______;
(5)所用盐酸盐溶液中溶质的质量分数______;
(6)恰好完全反应时所得溶液中溶质的质量分数______.
(2009?香坊区一模)复习时,常用专题探究的方法学习常见物质的组成、性质与制取,课堂上老师引导我们回顾了几个实验.
探究1:研究常见物质性质--氢氧化钠与硫酸是否刚好完全中和.
(1)探索:用玻璃棒蘸取反应后的溶液滴在pH试纸上,发现该溶液的pH<7,说明硫酸过量.
(2)验证:
写出 (2)中涉及的化学方程式______.
探究2:研究常见物质制取______制取氢氧化钠溶液.
甲同学向盛有澄清石灰水的烧杯中加入过量的碳酸钠溶液,生成白色沉淀,过滤后得到无色溶液,他说:“我制得了氢氧化钠溶液!”
乙同学却说:“这种无色溶液中不一定含有氢氧化钠.”他提出了如下实验:
丙同学认为乙的实验方案也不严密,不能证实无色溶液中一定含有氢氧化钠,理由是______.
丙同学设计了另一个实验:
我认为:显然丙同学的实验可靠性比甲、乙的实验好,原因是______.
探究1:研究常见物质性质--氢氧化钠与硫酸是否刚好完全中和.
(1)探索:用玻璃棒蘸取反应后的溶液滴在pH试纸上,发现该溶液的pH<7,说明硫酸过量.
(2)验证:
| 实验内容 | 实验现象 | 解释与结论 |
| 取少量反应后的溶液与试管中,加入锌粒 | ______ | 证明研究结论正确 |
探究2:研究常见物质制取______制取氢氧化钠溶液.
甲同学向盛有澄清石灰水的烧杯中加入过量的碳酸钠溶液,生成白色沉淀,过滤后得到无色溶液,他说:“我制得了氢氧化钠溶液!”
乙同学却说:“这种无色溶液中不一定含有氢氧化钠.”他提出了如下实验:
| 实验步骤 | 实验现象 | 实验结论 |
| 用试管取无色溶液少许,滴入2滴无色酚酞试液 | 无色酚酞试液变红 | 无色溶液中含有氢氧化钠 |
丙同学设计了另一个实验:
| 实验步骤 | 实验现象 | 实验结论 |
| ______ | ______ | 无色溶液中确实含有氢氧化钠 |