题目内容
 如图为KNO3、NaNO2(亚硝酸钠)、NaCl的溶解度曲线.请分析图象回答下列问题:
如图为KNO3、NaNO2(亚硝酸钠)、NaCl的溶解度曲线.请分析图象回答下列问题:(1)KNO3、NaNO2、NaCl三种物质受温度影响最大是
(2)60℃时,KNO3饱和溶液中溶质的质量分数
(3)NaNO2因外观与NaCl相似,经常会出现误食中毒的事件20℃时,取这两种固体各50g,分别加入到100g水中充分搅拌后,没有溶解完的固体是
考点:固体溶解度曲线及其作用,溶质的质量分数、溶解性和溶解度的关系
专题:溶液、浊液与溶解度
分析:(1)根据溶解度曲线可知三种物质的溶解度受温度的影响解答;
(2)根据60℃时KNO3与NaNO2的溶解度解答;
(3)根据20℃时NaNO2和NaCl的溶解度解答.
(2)根据60℃时KNO3与NaNO2的溶解度解答;
(3)根据20℃时NaNO2和NaCl的溶解度解答.
解答:解:
(1)根据溶解度曲线可知三种物质的溶解度受温度的影响最大的是硝酸钾;
故答案为:KNO3;
(2)60℃时KNO3与NaNO2的溶解度相等,根据饱和时质量分数的计算式
×100%可知:物质的溶解度相同则饱和溶液中溶质的质量分数也相同;
(3)观察溶解度曲线可知:20℃时NaNO2的溶解度大于NaCl的溶解度,且NaCl的溶解度小于50g,NaNO2的溶解度大于50g;所以20℃时,取两种固体各50g,分别加入到100g水中充分搅拌后,没有溶解完的固体是NaCl,NaNO2固体完全溶解依然不饱和;
答案:
(1)KNO3
(2)等于
(3)NaCl;不饱和.
(1)根据溶解度曲线可知三种物质的溶解度受温度的影响最大的是硝酸钾;
故答案为:KNO3;
(2)60℃时KNO3与NaNO2的溶解度相等,根据饱和时质量分数的计算式
| 溶解度 |
| 溶解度+100g |
(3)观察溶解度曲线可知:20℃时NaNO2的溶解度大于NaCl的溶解度,且NaCl的溶解度小于50g,NaNO2的溶解度大于50g;所以20℃时,取两种固体各50g,分别加入到100g水中充分搅拌后,没有溶解完的固体是NaCl,NaNO2固体完全溶解依然不饱和;
答案:
(1)KNO3
(2)等于
(3)NaCl;不饱和.
点评:本题考查了学生对溶解度曲线的认识和应用,较好的考查了学生分析、解决问题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
以下属于符号的是( )
A、 |
| B、F浮=G排液 |
C、 绿色食品 |
D、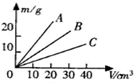 |
 如图所示的是电解水实验装置.通电一段时间后,在两个试管中分别收集到气体a和气体b.
如图所示的是电解水实验装置.通电一段时间后,在两个试管中分别收集到气体a和气体b.