题目内容
【题目】“x x”钙片主要成分是碳酸钙[化学式为:CaCO3]和维生素D。下图为商品标签图,请根据标签的有关信息,完成下列计算。
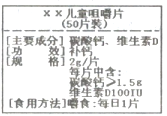
(1)碳酸钙中钙,碳,氧元素的质量比为多少?
(2)每盒钙片(以碳酸钙最少量计算)加足量稀盐酸反应可以制多少二氧化碳?
【答案】1)40:12:48或10:3:12
2)33g
【解析】(1)碳酸钙中钙,碳,氧元素的质量比=![]() =10:3:12;
=10:3:12;
(2)每片钙片中含碳酸钙的质量为1.5g,故每瓶钙片中含碳酸钙的质量为![]() =75g,设可生成二氧化碳的质量为x
=75g,设可生成二氧化碳的质量为x
CaCO3+2HCl == CaCl2+H2O+CO2↑
100 44
75g x
![]() =
=![]() 得x=33g
得x=33g
答:碳酸钙中钙,碳,氧元素的质量比10:3:12;每盒钙片(以碳酸钙最少量计算)加足量稀盐酸反应可以生成二氧化碳的质量为33g。

练习册系列答案
相关题目