题目内容
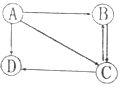
【题目】A、B、C三种物质的溶解度曲线如下图所示。
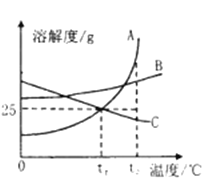
请回答下列问题:
(1)t1℃时A物质的溶解度是______。
(2)在t1℃时,将足量的三种物质的饱和溶液各恒温蒸发10g水后,它们析出的晶体的质量关系为______。
(3)在t2℃时,将质量均为25g的上述三种物质分别加入到100g水中,不能形成饱和溶液的是____。
(4)写出符合C曲线特点的两种物质的化学式_____,_____。
(5)将t2℃的这三种物质的饱和溶液分别降温至t1℃,所得溶液中溶质的质量分数从大到小的顺序是______。
【答案】25g B>A=C A、B CO2 Ca(OH)2 B>A>C
【解析】
(1)通过分析溶解度曲线可知,t1℃时A物质的溶解度是25g,故填25g;
(2)在t1℃时,B物质的溶解度最大,A、C物质的溶解度相等,所以将足量的三种物质的饱和溶液各恒温蒸发10g水后,它们析出的晶体的质关系为B>A=C,故填B>A=C;
(3)在t2℃时,A、B物质的溶解度大于25g,所以将质量均为25g的上述三种物质分别加入到100g水中,不能形成饱和溶液的是A、B,故填A、B;
(4)氢氧化钙和气体的溶解度随温度的升高而减小,所以符合C曲线特点的两种物质的化学式是:CO2,Ca(OH)2,故填CO2,Ca(OH)2;
(5)t1℃时,B物质的溶解度最大,A、C物质的溶解度相等,降低温度,A、B物质额溶解度减小,C物质的溶解度增大,应该按照t2℃时的溶解度计算,所以将t2℃的这三种物质的饱和溶液分别降温至t1℃,所得溶液中溶质的质量分数从大到小的顺序是B>A>C,故填B>A>C。

练习册系列答案
 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案
相关题目