题目内容
【题目】根据如图回答问题。
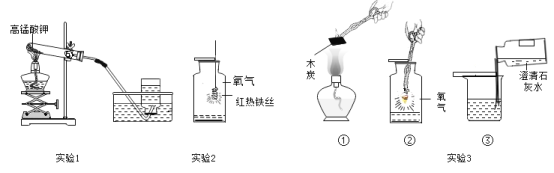
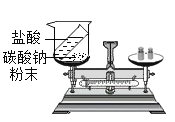
(1) 实验1中发生反应的化学方程式为______________________________,用排水法收集该气体的原因是_______________________________________。
(2)实验2的现象是___________________,集气瓶底放少量水的原因是_________。
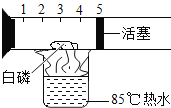
(3)实验3中,说明燃烧产物为二氧化碳的证据是______________(用化学方程式表示);对比①②可得到的结论是______________________________________。
【答案】![]() 该气体不易溶于水 剧烈燃烧,火星四射,生成黑色固体,放热 防止高温熔融物下落集气瓶底炸裂 Ca(OH)2+CO2=CaCO3↓+H2O 氧气浓度越大,木碳燃烧越剧烈
该气体不易溶于水 剧烈燃烧,火星四射,生成黑色固体,放热 防止高温熔融物下落集气瓶底炸裂 Ca(OH)2+CO2=CaCO3↓+H2O 氧气浓度越大,木碳燃烧越剧烈
【解析】
本题是对氧气的制取及性质进实验研究,要应用氧气制法、氧气具有的性质进解答。
(1)实验1中试管放入的药品为高锰酸钾,所以发生反应的化学方程式为![]() ,用排水法收集氧气的原因是氧气不易溶于水。
,用排水法收集氧气的原因是氧气不易溶于水。
(2)实验2是铁丝在氧气瓶中燃烧,现象是剧烈燃烧,火星四射,生成黑色固体,放热,由于生成物温度较高,所以集气瓶底放少量水防止高温熔融物下落集气瓶底炸裂。
(3)实验3中,说明燃烧产物为二氧化碳的证据是向气体滴加澄清石灰水,如果澄清石灰水变浑浊,则该气体为二氧化碳,所以方程式为Ca(OH)2+CO2=CaCO3↓+H2O;①是木炭在空气中燃烧,发出红光,放热;②是木炭在氧气中燃烧,剧裂燃烧,发出白光,放热。对比①②可得到的结论是氧气浓度越大,木碳燃烧越剧烈。

练习册系列答案
相关题目