题目内容
【题目】化学是从微观角度研究物质性质、组成、结构及其变化规律的科学。根据图示填空:
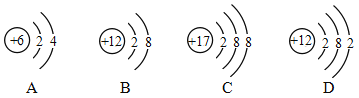
(1)图中A、B、C、D粒子共表示__________种元素。
(2)B与C所形成的化合物的化学式为______。
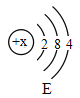
(3)晶体硅是制造半导体芯片的原料,如右图E是硅原子的结构示意图,图中x的值是__。
(4)硅元素的化学性质与A、B、C、D中__(填字母序号)元素的化学性质相似。
(5)“84消毒液”的成分为次氯酸钠(NaClO)、 氯化钠和水,其中NaClO为有效成分,写出氯气与氢氧化钠溶液反应制备“84消毒液”的化学方程式______。
【答案】三 MgCl2 14 A Cl2+2NaOH=NaCl+NaClO+H2O
【解析】
(1)图中A表示碳原子、B表示镁离子、C表示氯离子、D表示镁原子,粒子共表示碳、镁、氯三种元素。
(2)镁离子与氯离子所形成的化合物是氯化镁,化学式为:MgCl2。
(3)晶体硅是制造半导体芯片的原料,图E是硅原子的结构示意图,核内质子数=核外电子数,x=2+8+4,图中x的值是14。
(4)硅元素的化学性质与碳元素的化学性质相似,因为最外层电子数相等;
故选:A。
(5)氯气与氢氧化钠溶液反应产生氯化钠、次氯酸钠和水的化学方程式:Cl2+2NaOH=NaCl+NaClO+H2O。

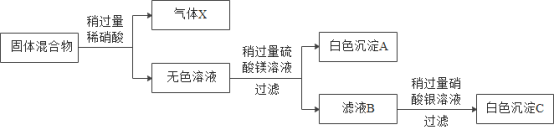
【题目】啤酒盖(主要成分为铁)生锈直接影响啤酒厂家的市场销售和品牌形象。某小组同学用铁钉代替啤酒盖模拟其生锈实验,探究铁生锈的条件及影响生锈速率的因素。
I.探究铁生锈的条件
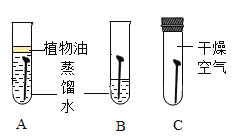

(1)证明铁生锈需要与氧气接触的实验现象是____。
II.探究影响铁生锈速率的因素
(查阅资料)啤酒的pH值大约在3.8~4.6之间
(猜想假设)铁钉生锈可能与溶液酸碱度、温度、是否杀菌有关。
实验1:分别取铁钉浸于等体积液体中,在空气中放置相同时间进行如下实验:
实验 | 是否杀菌 | pH值 | 温度/℃ | 锈蚀情况/% |
① | 杀菌 | 6 | 20 | 无现象 |
② | 杀菌 | 6 | 70 | 较明显生锈 |
③ | 未杀菌 | 6 | 70 | 明显生锈 |
④ | 未杀菌 | 6 | 20 | 略微生锈 |

实验2:在70℃时,将杀菌后的铁钉于等体积溶液中,在空气中放置相同时间进行如下实验:
实验 | Ⅰ | Ⅱ | Ⅲ | Ⅳ | Ⅴ |
pH值 | 3 | 5 | 7 | 9 | 11 |
锈蚀情况 | 完全生锈 | 明显生锈 | 略微生锈 | 无现象 | 无现象 |
(解释与结论):
(2)由实验1得出“温度与铁生锈速率有关”的结论,依据的两个实验是__(填编号)
(3)实验2的目的是_______。
(4)由实验1和实验2推知影响铁生锈的因素是_____
(反思与评价)
(5)实验2没有进行pH=13的实验,理由是 ___。
(6)结合本题请分析啤酒盖易生锈的原因是 ______
【题目】冬春季节是人感染禽流感的高发季节,采取预防措施非常重要。下表是应用于活禽市场中某种消毒液的主要成分:
用途 | 杀菌消毒 |
主要成分 | 硝酸、硝酸银、过氧化氢 |
请根据此表回答问题:
(1)该消毒液的溶剂为____;写出该消毒液中主要成分的化学式:___、___(任写两种)。
(2)该消毒液中含有的金属离子为_____。
(3)标出硝酸中氮元素的化合价:______。
【题目】请从A~D中任选三个作答,若均作答,按前三个计分。如图,在Y形管中进行实验。补全实验方案。
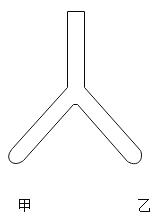
序号 | 目的 | 操作 | 现象 | 结论 |
A | 探究金属活动性 | 甲:放入铁片; 乙:放入银片; 向甲、乙处加入________ | 甲中有红色固体生成,溶液变为浅绿色; 乙中无明显变化 | 金属活动性:铁>铜> 银 |
B | 验证可燃物的燃烧条件 | 甲:放入红磷; 乙:放入白磷; 将甲、乙底部浸入80°C热水中 | 甲中无明显变化; 乙中白磷燃烧 | ________ |
C | 探究CO2的性质 | 甲:放入干燥的石蕊纸条; 乙:放入湿润的石蕊纸条; 向甲、乙处倒入CO2 | ________ | 二氧化碳能与水反应 |
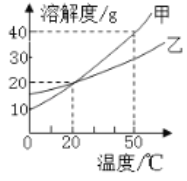
D | 比较________ | 甲:放入一小粒高锰酸钾; 乙:放入一小粒碘; 向甲、乙处加入等量蒸馏水 | 甲中固体溶解形成紫色溶液; 乙中固体几乎不溶解 | 相同条件下,高锰酸钾在水中的溶解能力比碘强 |
【题目】实验室制取气体时常要考虑下列问题:
(1)选择合理的制取装置。
用如下图所示装置制取气体,请回答下列问题。

①仪器a的名称是__。
②选用A加热KMnO4制O2,装置需要改进的地方是__,反应的化学方程式为__。
③实验室用Zn和稀硫酸制取H2的化学方程式为__。
④实验室可用亚硝酸钠(NaNO2)和NH4Cl的饱和溶液加热法制备N2,应选择的发生装置和收集装置的组合是__(写出一种组合,填序号)。
(2)检验、除杂和尾气处理。
①通过饱和NaHCO3溶液洗气,可除去CO2中的HCl。洗气时化学反应方程式为__。
②实验室制备下列气体时,一般需要进行尾气处理的是__(填序号)。
a H2 b CO c CO2 d SO2
(3)反应装置的改进和反应条件的探究。
某实验小组为了探究影响H2O2分解制取氧气快慢的因素,进行了下列实验:
实验序号 | H2O2溶液的质量分数/% | H2O2溶液的体积/ml | 温度/℃ | MnO2粉末的用量/g | 收集气体的体积/ml | 收集气体所需的时间/s |
A | 5 | 1 | 20 | 0.1 | 4 | a |
B | 15 | 1 | 20 | 0.1 | 4 | b |
C | 30 | 5 | 35 | 0.1 | 4 | c |
D | 30 | 5 | 55 | 0.1 | 4 | d |
①欲探究温度对H2O2分解快慢的影响,应该选择的对照实验组是__(填实验序号)。
②该小组利用如下左图所示装置探究MnO2质量对H2O2分解快慢的影响:在三份8.0ml3%的H2O2溶液中分别加入0.03g、0.06g和0.08gMnO2粉末,获得实验数据如下右图所示(温度变化忽略不计,产生氧气的体积与装置内的压强成正比)。通过对曲线图的分析,将推理得出的结论填写在下列空白中。

结论I:在其他条件不变的情况下,所用MnO2质量越大,H2O2的分解速率__。
结论II:在其他条件不变的情况下,所用MnO2质量越大,生成氧气的总量__。