题目内容
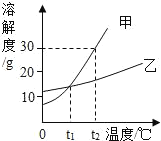
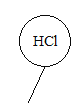
【题目】已知,同温、同压下,相同体积的任何气体都含有相同数目的分子。如图所示,相同状况下,分别用氯化氢和四种不同的混合气体吹出体积相等的五个气球。A、B、C、D四个气球中所含原子数与氯化氢气球中所含原子数一定相等的是( )
A. 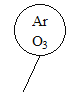 B.
B. 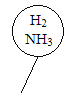 C.
C. 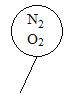 D.
D. 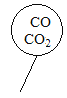
【答案】C
【解析】
相同条件下,气体的摩尔体积相同,根据![]() , 已知体积相同,故物质的量相同,设HCl为1mol,则原子为2mol。如果原子数相等,则原子的物质的量相等。
, 已知体积相同,故物质的量相同,设HCl为1mol,则原子为2mol。如果原子数相等,则原子的物质的量相等。
A、Ar为单原子分子、O3为三原子分子,二者体积比为1:1混合时,才符合,故错误;
B、H2为双原子分子、NH3为四原子分子,二者无论以何比例混合所含原子的物质的量均大于2mol,故错误;
C、N2为双原子分子、O2为双原子分子,二者无论以何比例混合所含原子的物质的量均等于2mol,故正确;
D、CO为双原子分子、CO2为三原子分子,二者无论以何比例混合所含原子的物质的量均大于2mol,故错误。
故选C。

 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案【题目】某化学活动小组用稀盐酸对方镁石中MgO含量进行测定(杂质不与盐酸反应且不溶于水),实验后得到一无色残液。为防止直接排放造成环境污染,对其组成进一步进行探究。
(活动一)过滤该残液,取10 g滤液,向其中不断加入5%的氢氧化钠溶液,所得实验数据如下表:
氢氧化钠溶液的质量/g | 4 | 8 | 12 | 16 | 28 | 32 |
生成沉淀的质量/g | 0 | 0 | 0.145 | 0.29 | 0.58 | 0.58 |
(1)通过对上述实验数据的分析,该滤液中含有的溶质是_____________(写化学式)。
(2)选择合理的数据,计算10 g滤液中溶质氯化镁的质量分数_____________(列出计算过程)。
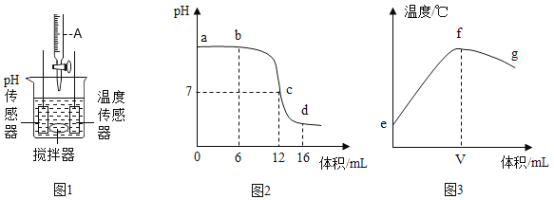
(活动二)小组同学将测得沉淀质量与所加入氢氧化钠溶液质量绘成坐标图如图所示。
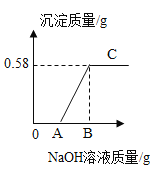
(3)A点时,溶液中溶质的化学式为____________;C点时溶液的pH _______7(填“>”“=”或“<”)。
(4)根据活动一的实验数据分析,A、B点的数值分别为_______、_______。
【题目】如表列出了①~⑥六种元素在周期表中的位置:
族 周期 | IA | |||||||
1 | IIA | IIIA | IVA | VA | VIA | VIIA | ||
2 | ① | ② | ||||||
3 | ③ | ④ | ⑤ | ⑥ | ||||
请按要求回答下列问题:
(1)元素①的元素符号是_____。
(2)元素⑤的原子结构示意图是_____。
(3)这六种元素中,位于第三周期且原子半径最小的是(填元素符号)_____。
(4)这六种元素中的金属元素组成的等质量的碳酸盐中,与足量稀盐酸反应放出CO2最多的碳酸盐的化学式为_____。
(5)在盛有硫酸铜溶液的小烧杯中加入元素③的单质,发生反应的现象是_____。