��Ŀ����
����Ŀ����1�����û�ѧ�������:
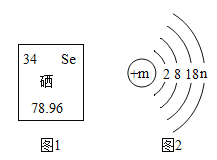
��3����ԭ��_____��
���Ȼ����е�������_____��
�۱��ֵ�����ѧ���ʵ���С����_____��
�ܹ�����������Ԫ�صĻ��ϼ�_____��
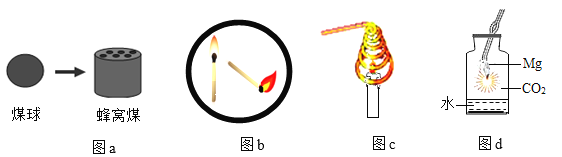
��2������7������:��Һ����̼����梨۳���ʯ��ˮ�ܽྻ�Ŀ����ݱ�ˮ����������آ�����þ���������ڻ�������_____��������ţ���ͬ�������ڴ��������_____�����ڵ��ʵ���_____��
���𰸡�3Ne Na+ N2 ![]() �ۢ� �٢ڢݢޢ� ��
�ۢ� �٢ڢݢޢ� ��
��������
��1������ԭ�ӵķ���ΪNe��3����ԭ��Ϊ��3Ne�������Ȼ����е�������Ϊ�����ӣ������ӱ�ʾΪ��Na+�����۱��ֵ�����ѧ���ʵ���С�����ǵ����ӣ�����������ԭ�ӹ��ɣ���ʾΪ��N2�����ܹ�����������Ԫ�صĻ��ϼ�δ+1�ۣ���ʾΪ��![]() ����
����
��2�����ڴ��������Һ����̼����李���ˮ��������ء�����þ���������dz���ʯ��ˮ���ྻ�Ŀ��������ڵ��ʵ���Һ����
�ʴ�Ϊ��3Ne��Na+��N2��![]() ���ۢܣ��٢ڢݢޢߣ��١�
���ۢܣ��٢ڢݢޢߣ��١�

 һ����������ϵ�д�
һ����������ϵ�д�����Ŀ��С��ͬѧ��ͨ��ʵ��̽��ij��ҵ���õİ���ƵĴ�����Ʒ�ijɷּ�������
[�������1]�ٸô�����Ʒ�к�����Щ����?
[���������]ͨ��������С���������¼��裺
(1)ֻ����Na2CO3��(2)����Na2CO3��NaHCO3
[��������]
NaHCO3 | Na2CO3 | |
����ϡ���� | ����I | �������� |
���뱥��ʯ��ˮ | ��Һ����� | ����� |
����CaCl2��Һ | ���������� | ��Һ����� |
������Һ�����ڣ�������ͨ�����ʯ��ˮ | ����ʯ��ˮ����� | ����ʯ��ˮ�����Ա仯 |
(1)���е������Ϊ___________��
(2)����I��Ӧ�Ļ�ѧ����ʽΪ_________��
[ʵ��̽��]Ϊ��ȷ��������Ʒ�ijɷ֣�С���������ʵ�鷽��������һ���������ʵ�鱨�档
ʵ�鲽�� | ʵ������ | |
��ȡ������Ʒ����ˮ�����������CaCl2��Һ | ��Һ����� | �÷�Ӧ�Ļ�ѧ����ʽ:___________�� |
�ڽ�������Ӧ��Ļ��Һ���ˣ�ȡ��Һ_______�� | _______�� | ֤������ڳ����� |
[ʵ�鷴˼]
ʵ�鲽����У������Լ�������Ŀ����_______��
[�������2]��β����ô�����Ʒ�и����ʵĺ���?

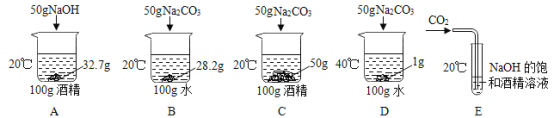
(1)Ϊ�����ô�����Ʒ���ɷֵĺ�����С���������ͼװ�ã�ͨ������Bװ���е������仯��ȷ����Ʒ�и��ɷֵĺ�������װ�����������ã�ϡ��������Ʒ������װ��B��CO2��NaOH����ȫ��Ӧ�������������ʵ�鷢�֣��ⶨ�����ƫ����ƫ���ԭ����
��__________����__________��
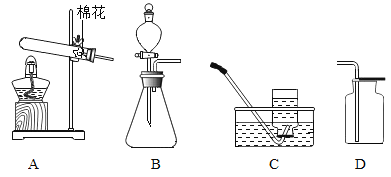
(2)С������ʦ��ָ����������������µ�ʵ��װ�á���ʵ�������²������裺

�ټ��װ�������ԣ��ڽ�w g�������Ʒ������ƿ�У�
�۳���ʢ����������Ũ��Һ��Bƿ������
�ܴ���b���ӵ���a������ע��һ�����Ŀ������رջ���b��
������ƿ����μ���ϡ���������ٲ������ݣ�
���ٴγ���ʢ����������Ũ��Һ��Bƿ������
����b���ӵ���a����������һ�����Ŀ������رջ���b��
�߸���Bƿ���ӵ�����������Ʒ�и��ɷֵĺ�����
��ʵ�����ȷ������___________��