题目内容
硫酸亚铁铵晶体化学式为xFeSO4•y(NH4)2SO4•zH2O,在制药、电镀方面有广泛的应用.
资料:①硫酸亚铁铵晶体易溶于水,不溶于乙醇;②硫酸亚铁铵晶体受热时,在200℃以下只有结晶水失去.

(探究一):制备硫酸亚铁铵晶体:学生用含有少量铜的废铁屑制备硫酸亚铁铵晶体,流程如图1:
(1)在盛有废铁屑的容器中,倒入热水和洗涤剂,充分搅拌.以除去废铁屑表面的油污,这是利用洗涤剂的_____作用;操作①中发生反应的化学方程式为_____;
(2)过滤所需的玻璃仪器有烧杯、玻璃棒、_____.过滤操作中滤纸有多种折法,为了加快过滤速率,你选择折法是_____;
(3)操作①中过滤时,要趁热进行说明:温度高,FeSO4溶解度___(大或小),过滤后得到的固体中一定含有的物质是__;
(4)操作②的目的是得到硫酸亚铁铵晶体.操作顺序是:b→_____→_____→d;
a.过滤 b.加热浓缩 c.冷却结晶 d.洗涤干燥
(5)操作②中使用乙醇洗涤,可快速晾干.这样做的优点是_____;
A、避免用水洗涤所造成的晶体损耗 B、酒精易挥发,可低温晾干晶体
(探究二):探究硫酸亚铁铵的组成
(实验步骤):取2份等质量的硫酸亚铁铵晶体,分别进行实验:向一份中加入过量的NaOH溶液,充分反应后得到0.68g NH3;向另一份中加入过量的BaCl2溶液,充分反应后过滤、洗涤、干燥得到9.32g沉淀.回答下列问题:
(6)实验中生成的NH3能使湿润的_____变蓝;写出(NH4)2SO4与NaOH反应的化学方程式:_____;
(7)取最后一次洗涤液,加入Na2SO4溶液,_____,则说明沉淀已经洗涤干净;根据实验数据,则x 和y的比值_____(相对分子质量:NH3﹣17、BaSO4﹣233);为进一步确定硫酸亚铁铵晶体的组成,另取7.84g硫酸亚铁铵晶体,并加热使其分解,剩余固体质量与温度的关系如图3所示,则:根据图示数据,硫酸亚铁铵晶体中,x:y:z=_____;
(8)写出A点到B点发生反应的化学方程式_____.
著名科学家居里夫人首先发现某些原子具有放射性,即原子能自动放射出一些粒子.一种元素的原子经过放射变成了另一种元素的原子,则此原子放射出的粒子一定是( )
A. 电子 B. 中子 C. 质子 D. 原子核
下列实验设计能达到目的是( )
选项 | A | B | C | D |
实验设计 |
|
|
|
|
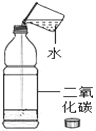
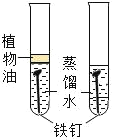
实验目的 | 证明二氧化碳与水反应生成碳酸 | 证明二氧化碳不可燃、不助燃、密度大于空气 | 证明可燃物燃烧需要氧气和温度达到着火点 | 证明铁生锈是水和氧气共同作用的结果 |
A. A B. B C. C D. D






 向一定量的稀硫酸中滴加氢氧化钠溶液至过量
向一定量的稀硫酸中滴加氢氧化钠溶液至过量 向一定量的H2SO4和MgSO4混合溶液中滴加氢氧化钡溶液
向一定量的H2SO4和MgSO4混合溶液中滴加氢氧化钡溶液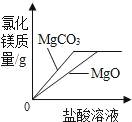 将足量MgCO3和MgO固体分别加入相同质量、相同质量分数的稀盐酸中
将足量MgCO3和MgO固体分别加入相同质量、相同质量分数的稀盐酸中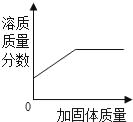 在一定温度下,向不饱和的硝酸钠溶液中不断加入硝酸钠固体,充分搅拌
在一定温度下,向不饱和的硝酸钠溶液中不断加入硝酸钠固体,充分搅拌 2Cu+CO2↑的反应,说法正确的是( )
2Cu+CO2↑的反应,说法正确的是( )