题目内容
某固体物质由MgSO4 和NaOH组成,取24g该固体混合物溶于水后,向所得的混合物中逐滴加入15%的硫酸,发现沉淀量y与加入密度为1.1g/cm3硫酸的体积x有下图表示的关系:
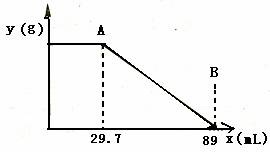
求该固体混合物中MgSO4 和NaOH各多少克?
解:图中A、B点硫酸质量:
A=1.1g/cm329.7mL15%=4.9g B=1.1g/cm389mL15%=14.7g)
用于跟Mg(OH)2反应的硫酸的质量为:14.7g-4.9g=9.8g)
设原混合物中MgSO4的质量为x
MgSO4 + 2NaOH = Na2SO4 + Mg(OH)2↓
Mg(OH)2 + H2SO4 = MgSO4 +2H2O
98 120
9.8 x
98/9.8=120/ x
x=12g
原混合物中NaOH的质量=24g-12g=12g

练习册系列答案
相关题目
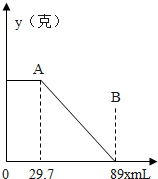

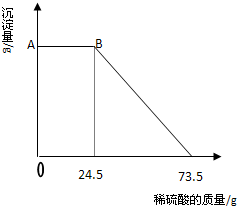 某固体物质由MgSO4和NaOH组成,取24g该固体混合物溶于水后,向所得的混合物中逐滴加入20%的稀硫酸,发现沉淀量与加入硫酸溶液的质量如图所示的关系.
某固体物质由MgSO4和NaOH组成,取24g该固体混合物溶于水后,向所得的混合物中逐滴加入20%的稀硫酸,发现沉淀量与加入硫酸溶液的质量如图所示的关系.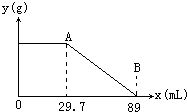 某固体物质由MgSO4和NaOH组成,取24.0g该固体混合物溶于水后,向所得的混合物中逐滴加入质量分数为15%的硫酸溶液(密度为1.1g?mL-1),加入的稀H2SO4的体积x(单位:mL)与所得沉淀质量y(单位;g)有如图所示的关系,求该固体混合物中NaOH、MgSO4的质量各为多少克?
某固体物质由MgSO4和NaOH组成,取24.0g该固体混合物溶于水后,向所得的混合物中逐滴加入质量分数为15%的硫酸溶液(密度为1.1g?mL-1),加入的稀H2SO4的体积x(单位:mL)与所得沉淀质量y(单位;g)有如图所示的关系,求该固体混合物中NaOH、MgSO4的质量各为多少克?