题目内容
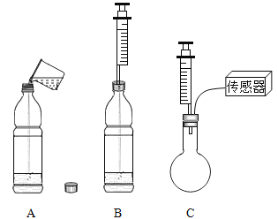
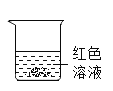
【题目】学习了生活中常见的盐后,化学实验活动课上,互助合作小组同学们做了如下图所示的三组实验。实验结束后,所有同学将A、B、C三支试管中的废液全部倒入一个干净的大烧杯中,静置一段时间,发现杯底有白色沉底,上层溶液呈红色 。
(提出问题)小明同学提出,大烧杯的上层溶液中除了含有水和酚酞外还含有哪些粒子?
(查阅资料) CaCl2溶液呈中性。
(猜想假设)经小组讨论后,同学们作了如下猜想:
①Na+、Cl- 、CO32-
②Na+、Cl-、OH-
③Na+、Cl-、 CO32-、OH-
④Na+、Cl-、Ca2+、OH-
⑤Na+、Ca2+、 CI-、CO32-
小明认为猜想______________不正确,理由是_______________。
(进行实验)同学们对可能存在的离子进行激烈的讨论,一组同学设计了如下方案,对可能存在的粒子进行探究。
实验操作 | 实验现象 | 实验结论 |
取废液少许于试管中,向其中滴加过量的CaCl2溶液 | ____________ | 溶液中一定含有CO32- |
试管中上层清液仍为红色 | 溶液中一定含有_____(写离子符号) |
实验中加入过量的CaCl2溶液的目的是___________________。
(得出结论)猜想___________________正确。
(反思提升)探究废液成分时,需先分析出一定存在和一定不存在的离子,然后再对________进行检验。
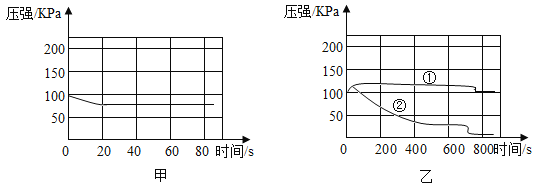
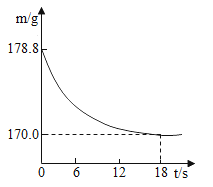
(拓展延伸)某纯碱样品中含有少量氯化钠杂质。称取该样品22. 8g,加入到盛有一定质量稀盐酸的烧杯中,碳酸钠与稀盐酸恰好完全反应,气体完全逸出,得到不饱和NaCl溶液。反应过程中测得烧杯内混合物的质量(m)与反应时间(t)关系如图所示。计算所得溶液中溶质的质量分数。(写出解题过程,计算结果精确到0. 1%)________________________
【答案】⑤ Ca2+和CO32-不能共存。 有白色沉淀产生 OH-。 检验并除去CO32- ③ 可能存在的离子 14.7%
【解析】
猜想假设:
猜想⑤不正确,理由是钙离子和碳酸根离子不能共存。
进行实验
取废液少许于试管中,向其中滴加过量的CaCl2溶液,产生白色沉淀,是因为碳酸根离子和钙离子结合生成白色沉淀碳酸钙;
试管中上层清液仍为红色,说明溶液显碱性,加入过量的氯化钙溶液后,碳酸根离子消失,因此能使溶液变红色的是氢氧根离子,因此溶液中含有氢氧根离子;实验中加入过量的CaCl2溶液的目的是检验并且除去碳酸根离子。
得出结论:
由以上分析可知,溶液中含有钠离子、氯离子、碳酸根离子、氢氧根离子,猜想③正确。
反思提升:
探究废液成分时,需先分析出一定存在、一定不存在和可能存在的离子,然后再对可能存在的离子进行检验。
由图像和质量守恒定律可知,生成二氧化碳的质量为:178.8g﹣170.0g=8.8g;
设碳酸钠的质量为x,生成氯化钠的质量为y,
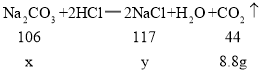
![]()
![]()
解得:x=21.2g,y=23.4g,
原样品中氯化钠质量为![]()
完全反应后所得氯化钠溶液的溶质质量分数为![]()

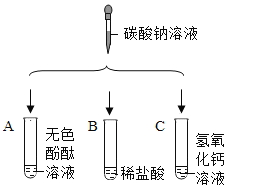
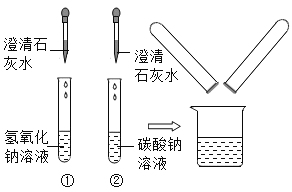
【题目】在化学实验技能考试中,有一题目是鉴别碳酸钠溶液和氢氧化钠溶液,小红等几位同学进行了如下图所示的实验。
(1)实验中,无明显变化的试管是___________(填编号)。
(2)实验结束后,小红同学将①、②两支试管中的废液倒入同一个干净的烧杯中,看到废液浑浊,就对废液进行了过滤,小红等几位同学对滤液的成分又进行了探究。
(提出问题)滤液中除水外还含有哪些物质?
(猜想)小红认为:只含氢氧化钠;
小明认为:可能含有氢氧化钠、碳酸钠和氢氧化钙;
小亮认为:可能含有氢氧化钠和碳酸钠;
你认为还可能是 ______________________ (写一种猜想)。
(讨论)你认为小红、小明、小亮三位同学中谁的猜想不合理,请说明理由:___________。
(实验设计)设计一个简单的实验证明你的猜想正确。
实验步骤 | 实验现象 | 实验结论 |
取样于试管中:______________ | 试管中出现白色浑浊 | 你的猜想正确 |
(实验分析)小亮同学针对自己的猜想进行了如下实验:
实验步骤 | 实验现象 | 实验结论 |
取样于试管中,滴入几滴稀盐酸 | 没有气泡产生 | 自己的猜想不成立 |
你认为小亮同学对实验结果判断是否正确?请说明理由。____________________。
(反思拓展)
①在分析化学反应后所得物质的成分时,除考虑生成物外还需考虑__________________________;
②通过以上探究,你认为应怎样处理上述实验后的废液才能倒入下水道?_____________________。