题目内容
【题目】人们曾用贝壳(主婴成分是碳酸钙,杂质不参与反应且不溶于水) 和纯碱为原材料制取烧碱,制取流程如图所示。
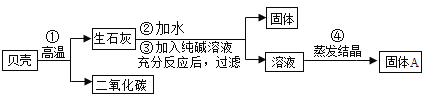
(1)写出步骤①的反应化学方程式_____
(2)固体 A 的成分可能是纯净的氢氧化钠,还可能是_________、_____(填化学式)。
【答案】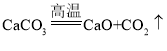 NaOH和Na2CO3 NaOH和Ca(OH)2
NaOH和Na2CO3 NaOH和Ca(OH)2
【解析】
(1)贝壳主要成分是碳酸钙,碳酸钙高温分解生成水和二氧化碳,反应的化学方程式为: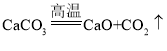
(2)步骤②的反应为:CaO+H2O=Ca(OH)2,步骤③的反应为:
Na2CO3+Ca(OH)2 =CaCO3↓+2NaOH,步骤③中,如果碳酸钠有剩余,固体 A 的成分是NaOH和Na2CO3;步骤③中,如果氢氧化钙有剩余,固体 A 的成分是NaOH和Ca(OH)2。

【题目】氢氧化钾是工业强碱之一,与氢氧化钠化学性质相似。一次化学实验后同学忘记盖瓶塞。化学兴趣小组同学想探究该瓶氢氧化钾固体是否变质。大家展开充分讨论,邀你参与。
(猜想)A、没有变质
B、部分变质
C、完全变质
(1)氢氧化钾在空气中变质的原因____(用方程式表示)。
(査阅资料)氯化钾溶液和氯化钙溶液呈中性。
(2)设计甲、乙两组实验方案并完成实验取瓶中固体少许,加水溶解配成溶液,分装于两支洁净试管。
实验方案 | 实验操作 | 实验现象 | 实验结论 |
甲 | 取一支试管,滴入无色酚酞试液,振荡 | 溶液变红色 | 猜想A正确 |
乙 | 取另一支试管,滴入足量的氯化钙溶液充分反应后再滴入几滴硫酸铵试液 | 先有___产生 再有____产生 | 猜想B正确 |
(3)(相互交流)大家认为甲的方案不可信,请你说出理由_____。滴入硫酸铵后发生的化学反应方程式_____。
(4)如果B猜想是正确的,大家想继续探究该瓶氢氧化钾固体中KOH的质量分数。设计了下列实验。
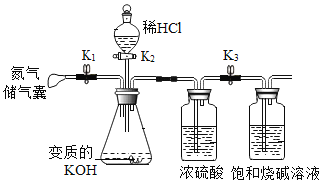
(操作步骤)①首先称量出饱和烧碱溶液(含仪器)的质量m1再与前面装置连接。
②按正确方法检查装置气密性,气密性良好。
③关闭K2,打开K1和K3,挤压N2储气囊给装置充分充气。
④关闭K1,打开K2滴入足量稀HCl,充分反应。⑤关闭K2,打开K1再次挤压N2储气囊,给装置充分充气。⑥关闭K3取下盛装烧碱的装置,称量质量为m2。回答问题:
(Ⅰ)步骤③充入N2的目是_____。
(Ⅱ)浓硫酸的作用是_______。
(Ⅲ)若不进行步骤⑤,KOH质量分数(偏大或偏小)____。
【题目】啤酒盖(主要成分为铁)生锈直接影响啤酒厂家的市场销售和品牌形象。某小组同学用铁钉代替啤酒盖模拟其生锈实验,探究铁生锈的条件及影响生锈速率的因素。
I.探究铁生锈的条件
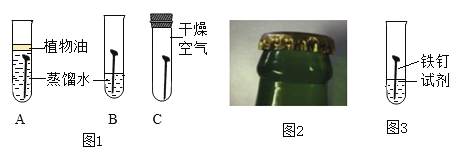
(1)证明铁生锈需要与氧气接触的实验现象是____________。
Ⅱ.探究影响铁生锈速率的因素
(查阅资料)啤酒的pH值大约在3.8~4.6之间。
(猜想假设)铁钉生锈可能与溶液酸碱度、温度、是否杀菌有关。
实验1
分别取铁钉浸于等体积液体中,在空气中放置相同时间进行如下实验:
实验 | 是否杀菌 | pH值 | 温度/℃ | 锈蚀情况/% |
1 | 杀菌 | 6 | 20 | 无现象 |
2 | 杀菌 | 6 | 70 | 较明显生锈 |
3 | 未杀菌 | 6 | 70 | 明显生锈 |
4 | 未杀菌 | 6 | 20 | 略微生锈 |
实验2
在70℃时,将杀菌后的铁钉于等体积溶液中,在空气中放置相同时间进行如下实验:
实验 | Ⅰ | Ⅱ | Ⅲ | Ⅳ | Ⅴ |
pH值 | 5 | 7 | 9 | 11 | |
锈蚀情况 | 完全生锈 | 明显生锈 | 略微生锈 | 无现象 | 无现象 |
(解释与结论):
(2)由实验1得出“温度与铁生锈速率有关”的结论,依据的两个实验是___________(填编号)。
(3)实验2的目的是____________。
(4)由实验1和实验2推知影响铁生锈的因素是______________。
(5)实验2没有进行pH=13的实验,理由是______________。
(6)结合本题请分析啤酒盖易生锈的原因是_____________。
(反思与评价)
如图所示实验探究铁生锈的条件(每支试管中均放有完全相同的洁净铁片):

(1)甲同学认为,试管A发生的现象就能够说明铁的锈蚀是铁与空气中的氧气、水蒸气共同作用的结果.乙同学不同意他的观点,认为必须全面观察试管____________(选填试管编号)发生的现象,并经过科学严谨的推理,才能得出上述结论.
(2)试管D和E实验的目的是_____________的环境中是否更容易锈蚀.
(3)通过本次探究活动,你有哪些收获和体会?______________