题目内容
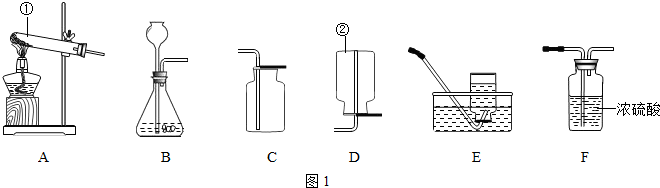
实验室制取二氧化碳一般有五个步骤:①检查装置的气密性;②按要求装好仪器; ③向长颈漏斗中注入稀盐酸;④向反应容器中放入几小块大理石;⑤收集气体.其正确顺序是( )
分析:根据制取二氧化碳的步骤进行解答,可概括为:连--查--加--倒--定--收.
解答:解:制取二氧化碳的操作步骤是:连(连接仪器、组装实验装置)→查(检查装置的气密性)→加(加入固体药品)→倒(倒入液体药品)→定(用铁架台固定仪器装置)→收集(用向上排空气法,导管要伸到集气瓶的底部,且瓶口还要盖上玻璃片).
故选B.
故选B.
点评:本题主要考查了实验室制取二氧化碳的实验步骤,细心操作,规范实验,了解相关知识是解答的关键.

练习册系列答案
相关题目