题目内容
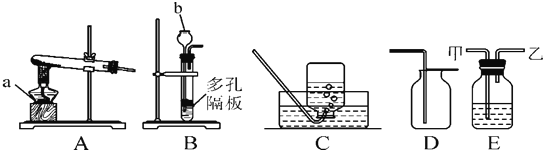
【题目】将暗紫色(或紫红色)的固体A加热,产生一种无色无味的气体B;取淡黄色粉末C点燃放入B中,产生明亮的蓝紫色火焰,生成一种有刺激性气味的气体D,将E引燃放入B中火星四射,生成一种黑色固体.试回答:
①写出上述物质的名称:A_________,B_________,C________,D________,E_________.
②写出上述有关的反应的文字表达式,在后面的括号写出其反应类型:
(1)________________________(________)
(2)________________________(________)
(3)________________________(________)
【答案】 高锰酸钾 氧气 硫 二氧化硫 四氧化三铁 2KMnO4![]() K2MnO4+MnO2+O2↑ 分解反应 S+O2
K2MnO4+MnO2+O2↑ 分解反应 S+O2![]() SO2, 化合反应 3Fe+2O2
SO2, 化合反应 3Fe+2O2![]() Fe3O4 化合反应
Fe3O4 化合反应
【解析】暗紫色固体A加热后产生一种无色无味的气体B,把淡黄色粉末C加热后放入盛有B的集气瓶中,发出明亮蓝紫色火焰,同时生成一种有刺激性气味的气体的D,故B是氧气,C是硫,D是二氧化硫,A是高锰酸钾;E引燃放入B中火星四射,生成一种黑色固体,故E是铁;
①A是高锰酸钾,B是氧气,C是硫,D是二氧化硫,E是四氧化三铁,故填:高锰酸钾,氧气,硫,二氧化硫,四氧化三铁;
②(1)高锰酸钾受热能分解生成锰酸钾、二氧化锰和氧气,属于分解反应,故填:2KMnO4![]() K2MnO4+MnO2+O2↑,分解反应;
K2MnO4+MnO2+O2↑,分解反应;
(2)硫在氧气中燃烧生成二氧化硫,属于化合反应,故填:S+O2![]() SO2,化合反应;
SO2,化合反应;
(3)铁在氧气中燃烧生成四氧化三铁,属于化合反应,故填:3Fe+2O2![]() Fe3O4,化合反应.
Fe3O4,化合反应.

 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案【题目】用不纯的锌片(杂质不参加反应)与稀硫酸反应,六次实验结果记录如下:(计算结果均取整数)

次数 | 1 | 2 | 3 | 4 | 5 | 6 |
加入锌的质量(g) | 2 | 4 | 6 | 8 | 10 | 12 |
稀硫酸的质量(g) | 60 | 60 | 60 | 60 | 60 | 60 |
生成的硫酸锌的质量(g) | 5 | 15 | 17 | 17 |
(1)将第2次和第5次实验产生的硫酸锌的质量填在上表中;
(2)在右图中画出硫酸锌与锌的质量函数关系的曲线;
(3)若将(10+m)g这种锌片放入60g这种稀硫酸中,充分反应后剩余固体的质量为 g;
(4)该实验所使用的稀硫酸中溶质的质量分数为 .