题目内容
某同学在敞口容器中做了两个实验:一是氧化汞(HgO)受热分解生成汞和氧气;二是铁粉在氧气中燃烧生成黑色固体.他准确称量了反应前后容器及所盛物质的质量,发现反应前后质量都反应了变化.请填空:
①铁粉燃烧生成四氧化三铁的质量比参加反应铁粉的质量
②你认为这两个反应是否遵循质量守恒定律?
③请写出题中涉及的化学方程式:
(2)下图是甲烷燃烧的微观模拟图,请回答下列问题: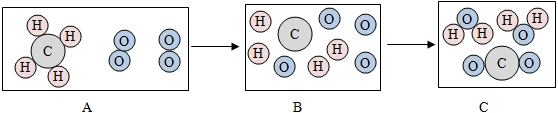
①在点燃的条件下,A到B的过程表示的是甲烷分子分解成碳原子和氢原子,氧分子分解成氧原子,B到C的过程表示的是
②该反应的化学方程式为
并请你分析:在上述三个化学反应中,反应前后,一定不会改变的是
A、物质的种类 B、元素的种类 C、原子的种类 D、分子的种类 E、分子的数目 F、原子的数目.
①铁粉燃烧生成四氧化三铁的质量比参加反应铁粉的质量
大
大
(选填“大”、“小”或“不变”).②你认为这两个反应是否遵循质量守恒定律?
是
是
(选填“是”或“否”).③请写出题中涉及的化学方程式:
2HgO
2Hg+O2↑
| ||
2HgO
2Hg+O2↑
;
| ||
3Fe+2O2
Fe3O4
| ||
3Fe+2O2
Fe3O4
.
| ||
(2)下图是甲烷燃烧的微观模拟图,请回答下列问题:

①在点燃的条件下,A到B的过程表示的是甲烷分子分解成碳原子和氢原子,氧分子分解成氧原子,B到C的过程表示的是
一个碳原子和两个氧原子结合成二氧化碳分子,一个氧原子和两个氢原子结合成一个水分子
一个碳原子和两个氧原子结合成二氧化碳分子,一个氧原子和两个氢原子结合成一个水分子
;②该反应的化学方程式为
CH4+2O2
CO2+2H2O
| ||
CH4+2O2
CO2+2H2O
.
| ||
并请你分析:在上述三个化学反应中,反应前后,一定不会改变的是
BCF
BCF
(填序号).A、物质的种类 B、元素的种类 C、原子的种类 D、分子的种类 E、分子的数目 F、原子的数目.
分析:(1)质量守恒定律的内容是:参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和.铁粉在氧气中燃烧生成四氧化三铁,四氧化三铁的质量大于铁粉的质量;化学变化都遵守质量守恒定律;根据化学方程式的书写分析;
(2)图B中的每2个氢原子与1个氧原子结合成水分子,每个碳原子与2个氧原子结合成二氧化碳分子,据此可写出反应的化学方程式.
(2)图B中的每2个氢原子与1个氧原子结合成水分子,每个碳原子与2个氧原子结合成二氧化碳分子,据此可写出反应的化学方程式.
解答:解:(1)①铁粉在氧气中燃烧生成四氧化三铁,四氧化三铁的质量大于铁粉的质量;故答案为:大;
②化学变化都遵守质量守恒定律,故答案为:是;
③氧化汞(HgO)受热分解生成汞和氧气,反应的化学方程式是2HgO
2Hg+O2↑;铁粉在氧气中燃烧生成黑色固体,反应的化学方程式是3Fe+2O2
Fe3O4;
(2)①图B中的每2个氢原子与1个氧原子结合成水分子,每个碳原子与2个氧原子结合成二氧化碳分子.故答案为:一个碳原子和两个氧原子结合成二氧化碳分子,一个氧原子和两个氢原子结合成一个水分子;
②该反应为每个甲烷分子与两个氧分子反应,生成两个水分子和一个二氧化碳分子,故反应的化学方程式为CH4+2O2
CO2+2H2O;化学反应中,反应前后一定不会改变的是原子种类、原子数目、元素种类.故答案为:CH4+2O2
CO2+2H2O;BCF.
②化学变化都遵守质量守恒定律,故答案为:是;
③氧化汞(HgO)受热分解生成汞和氧气,反应的化学方程式是2HgO
| ||
| ||
(2)①图B中的每2个氢原子与1个氧原子结合成水分子,每个碳原子与2个氧原子结合成二氧化碳分子.故答案为:一个碳原子和两个氧原子结合成二氧化碳分子,一个氧原子和两个氢原子结合成一个水分子;
②该反应为每个甲烷分子与两个氧分子反应,生成两个水分子和一个二氧化碳分子,故反应的化学方程式为CH4+2O2
| ||
| ||
点评:本考点是有关质量守恒定律的实验探究和化学方程式的书写,有关质量守恒定律的考题在中考中经常出现,要抓住要点:五个一定不变,一个一定变.还要注意药品的选择和装置的选择、反应容器的严密性等,本考点经常出现在选择题、填空题和实验题中.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
 质量守恒定律的定量研究对化学科学发展具有重大意义.
质量守恒定律的定量研究对化学科学发展具有重大意义. ”和“
”和“ ”分别表示两种不同的原子:
”分别表示两种不同的原子: ”聚集成的物质
”聚集成的物质