题目内容
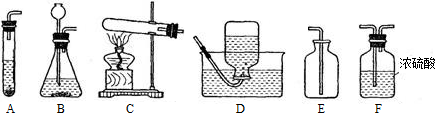
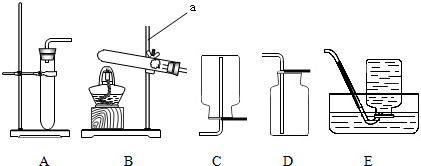
某化学兴趣小组用下图所示装置(省略了夹持装置)做如下实验:
研究课题:探究食品保鲜袋的元素组成.
查阅资料:碱石灰是由氢氧化钠和氧化钙组成的吸收剂;无水硫酸铜可作为吸水剂,且吸水后显蓝色.
提出猜想:制保鲜袋的材料可能是由“碳、氢、氧”中两种或三种元素组成.
实验步骤:
①按图示连接好仪器,将止水夹夹在F后的橡胶管处,B中注入适量水,当向A中缓缓注入少量水时,观察到装置B中的现象为X______,说明装置的气密性良好.
②按图示装好药品和1.4g剪碎的保鲜袋样品,除D、E、F、止水夹外将仪器按原样组装.
③向A中缓慢注水一段时间后,将已称重的D、E两干燥管和未称重F干燥管接到C的尾端.④给装置C加热,直至保鲜袋碎片完全燃烧.
⑤停止加热并继续向A中注水一段时间.
⑥分别对D、E进行第二次称重.
实验分析:
(1)根据实验原理分析,该套装置中缺少的玻璃仪器是______.
(2)实验步骤①中,观察到的现象为______.
(3)设置F处的干燥管的目的是______.B处的浓硫酸起的作用是______,如果没有B则对实验结果的影响是______.
(4)在加热装置C前,要向A中缓慢注水一段时间是为了______.停止加热后继续向A中缓慢注水一段时间是为了______.
(5)第一次对D、E称重质量分别为82.0g、85.0g;第二次对D、E称重质量分别为83.8g、89.4g;则样品完全燃烧后产生水的质量为______g.
实验结论:
(6)该样品的组成元素一定是______.
【答案】分析:(1)根据实验原理分析,反应需要加热;
(2)检查装置的气密性:按图示连接好仪器,将止水夹夹在F后的橡胶管处,B中注入适量水,当向A中缓缓注入少量水时,观察到装置B中的现象;
(3)根据资料“碱石灰是由氢氧化钠和氧化钙组成的吸收剂;无水硫酸铜可作为吸水剂,且吸水后显蓝色”,了解F、B的装置作用;
(4)“③向A中缓慢注水一段时间后”,“⑤停止加热并继续向A中注水一段时间”注水的目的;
(5)根据“第一次对D、E称重质量分别为82.0g、85.0g;第二次对D、E称重质量分别为83.8g、89.4g”,则可计算样品完全燃烧后产生水的质量;
(6)通过计算,生成水的质量为1.8克,生成二氧化碳的质量为4.4克,则可推测其元素组成.
解答:解:实验分析:
(1)根据实验原理分析,该套装置中缺少的玻璃仪器是:酒精灯.
(2)实验步骤①中,观察到的现象为:G处液柱上升.
(3)设置F处的干燥管的目的是:防止装置外空气中的CO2和H2O被E吸收,影响实验.B处的浓硫酸起的作用是:干燥氧气或除去水蒸气,如果没有B则对实验结果的影响是:使氢元素质量偏大或使水的质量偏大.
(4)在加热装置C前,要向A中缓慢注水一段时间是为了:将装置中的空气排尽.停止加热后继续向A中缓慢注水一段时间是为了:将生成的二氧化碳和水驱赶至D、E装置中被完全吸收.
(5)因为第一次对D、E称重质量分别为82.0g、85.0g;第二次对D、E称重质量分别为83.8g、89.4g;则样品完全燃烧后产生水的质量为83.8-82.0=1.8克.
实验结论:
(6)通过计算,生成水的质量为1.8克,生成二氧化碳的质量为4.4克,则该样品的组成元素一定是:C、H.
故答为:(1)酒精灯;
(2)G处液柱上升;
(3)防止装置外空气中的CO2和H2O被E吸收,影响实验;干燥氧气或除去水蒸气;使氢元素质量偏大或使水的质量偏大;
(4)将装置中的空气排尽;将生成的二氧化碳和水驱赶至D、E装置中被完全吸收;
(5)1.8g;
(6)C、H.
点评:本题考查了物质的组成和构成,注意宏观概念和微观概念描述上的差别,注意利用实验数据及其计算方法.
(2)检查装置的气密性:按图示连接好仪器,将止水夹夹在F后的橡胶管处,B中注入适量水,当向A中缓缓注入少量水时,观察到装置B中的现象;
(3)根据资料“碱石灰是由氢氧化钠和氧化钙组成的吸收剂;无水硫酸铜可作为吸水剂,且吸水后显蓝色”,了解F、B的装置作用;
(4)“③向A中缓慢注水一段时间后”,“⑤停止加热并继续向A中注水一段时间”注水的目的;
(5)根据“第一次对D、E称重质量分别为82.0g、85.0g;第二次对D、E称重质量分别为83.8g、89.4g”,则可计算样品完全燃烧后产生水的质量;
(6)通过计算,生成水的质量为1.8克,生成二氧化碳的质量为4.4克,则可推测其元素组成.
解答:解:实验分析:
(1)根据实验原理分析,该套装置中缺少的玻璃仪器是:酒精灯.
(2)实验步骤①中,观察到的现象为:G处液柱上升.
(3)设置F处的干燥管的目的是:防止装置外空气中的CO2和H2O被E吸收,影响实验.B处的浓硫酸起的作用是:干燥氧气或除去水蒸气,如果没有B则对实验结果的影响是:使氢元素质量偏大或使水的质量偏大.
(4)在加热装置C前,要向A中缓慢注水一段时间是为了:将装置中的空气排尽.停止加热后继续向A中缓慢注水一段时间是为了:将生成的二氧化碳和水驱赶至D、E装置中被完全吸收.
(5)因为第一次对D、E称重质量分别为82.0g、85.0g;第二次对D、E称重质量分别为83.8g、89.4g;则样品完全燃烧后产生水的质量为83.8-82.0=1.8克.
实验结论:
(6)通过计算,生成水的质量为1.8克,生成二氧化碳的质量为4.4克,则该样品的组成元素一定是:C、H.
故答为:(1)酒精灯;
(2)G处液柱上升;
(3)防止装置外空气中的CO2和H2O被E吸收,影响实验;干燥氧气或除去水蒸气;使氢元素质量偏大或使水的质量偏大;
(4)将装置中的空气排尽;将生成的二氧化碳和水驱赶至D、E装置中被完全吸收;
(5)1.8g;
(6)C、H.
点评:本题考查了物质的组成和构成,注意宏观概念和微观概念描述上的差别,注意利用实验数据及其计算方法.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目