题目内容
【题目】下面是几种粒子的结构示意图:
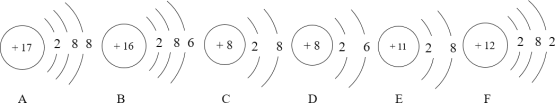
(1)上述粒子中,属于同种元素的是______,该元素位于元素周期表的第_________周期;
(2)上述粒子中,化学性质相似的原子是______,表示阳离子的是__________;
(3)A 与 F 所表示的元素组成的化合物名称是_____________,该化合物中 A、F 元素质量比为________________。
【答案】CD 二 BD E 氯化镁 71:24
【解析】
(1)上述粒子中,属于同种元素的是CD,它们质子数相同,该元素位于元素周期表的第二周期;
(2)上述粒子中,化学性质相似的原子是BC,它们最外层电子数相同,表示阳离子的是E,其核电荷数大于核外电子数;
(3)A 表示氯离子, F 表示镁原子,氯元素和镁元素组成的化合物名称是氯化镁,化学式为![]() ,该化合物中 A(氯)、F (镁)元素质量比为
,该化合物中 A(氯)、F (镁)元素质量比为![]() 。
。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】化学兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验(图一)。
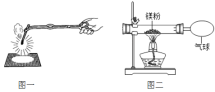
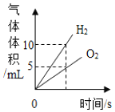
(1)请写出镁条与氧气反应的化学方程式_____________。
(2)经测量发现燃烧产物的质量_______(填“大于”“小于”或“等于”)镁条的质量,分析可知出现这一结果的原因是_________。
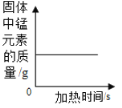
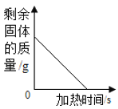
(3)兴趣小组按图二装置改进实验后,验证了质量守恒定律,同时发现燃烧产物中有少量黄色固体。
(提出问题)黄色固体是什么呢?
(查阅资料)①氧化镁为白色固体,常温下与水不反应;②镁能与氮气反应生成黄色的氮化镁(Mg3N2)固体;③氮化镁可与水剧烈反应产生氨气,该气体能使湿润的红色石蕊试纸变蓝。
(做出猜想)黄色固体为Mg3N2
(进行实验)同学们通过实验对猜想进行了验证,请你将实验记录表补充完整
实验操作 | 实验现象 | 结论 |
将镁粉燃烧的产物放在一只试管中,加入少量的蒸馏水,然后将一湿润的红色石蕊试纸放在试管口,观察现象 | _______ | 黄色固体 为氮化镁 |
(反思与交流)空气中氮气的含量远大于氧气的含量,而镁条在空气中燃烧生成的氧化镁却远多于氮化镁,是因为 ___________。镁条_________(填“能”或“不能”)代替红磷做测定空气中氧气含量的实验,因为________________。