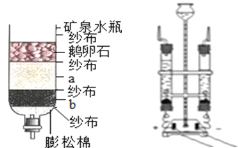
题目内容
【题目】实验室有失去标签的两瓶无色溶液,分别是氢氧化钡溶液和稀硫酸。为了鉴别它们设计如下鉴别方法:先把两瓶溶液分别贴上标签A、B,然后进行实验。
加入的试剂 | 实验现象 | 实验结论 | |
方法1 | 锌粒 | A中无明显现象 B中产生气泡 | A是______溶液; B是______溶液 |
方法2 | 碳酸钠溶液 | A中______; B中______。 |
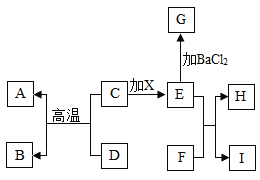
化学小组同学对方法2进一步探究,设计了如下实验方案
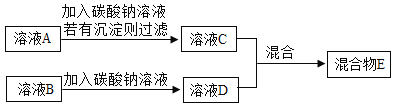
溶液C和溶液D混合,可能有以下三种情况:
(1)若有气泡产生,写出反应的化学方程式______;
(2)若有沉淀产生,通过现象可推出溶液C中的溶质是______;
(3)若无明显现象,混合物E中所含溶质种类最多时,写出所有溶质的化学式______。
【答案】产生沉淀 产生气泡 氢氧化钡 硫酸 H2SO4+Na2CO3=Na2SO4+H2O+CO2↑ 氢氧化钠、氢氧化钡 NaOH、Na2SO4、Na2CO3
【解析】
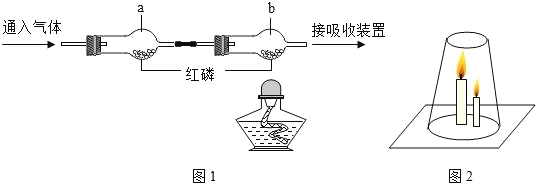
方法2:通过方法1的实验现象可知,a是氢氧化钡溶液;b是稀硫酸;所以分别加入碳酸钠溶液,a中的现象是有白色沉淀生成;b中现象是有气泡冒出;故填:
加入的试剂 | 实验现象 | 实验结论 | |
方法1 | 锌粒 | A中无明显现象 B中产生气泡 | A是 氢氧化钡 溶液; B是 硫酸 溶液 |
方法2 | 碳酸钠溶液 | A中产生白色沉淀 ; B中 产生气泡 。 |
(1)若有气泡产生,说明溶液c中有碳酸钠,溶液d中有硫酸,化学方程式为: H2SO4+Na2CO3=Na2SO4+H2O+CO2↑; 故填:H2SO4+Na2CO3=Na2SO4+H2O+CO2↑
(2)若有沉淀产生,说明溶液c中有剩余氢氧化钡和生成的氢氧化钠;故填:氢氧化钠、氢氧化钡
(3)若无明显现象,则c中含有氢氧化钠、碳酸钠,d中含有硫酸钠会使e中含有的溶质最多,故填: NaOH、Na2SO4、Na2CO3

 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案【题目】为测定硫酸钠和硫酸镁固体混合物中硫酸镁的质量分数。某同学取固体混合物26.2g,向其中加入219.6g水,使其完全溶解配制成混合溶液。将200g一定溶质质量分数的氢氧化钠溶液平均分成5等份,依次加入到上述混合溶液中,生成沉淀的质量与加入氢氧化钠溶液的质量关系如下表:
次数 | 第一次 | 第二次 | 第三次 | 第四次 | 第五次 |
氢氧化钠溶液质量/g | 40 | 40 | 40 | 40 | 40 |
产生沉淀质量/g | 1.45 | 2.9 | m | 5.8 | 5.8 |
试分析计算。
(1)m的值为_____。
(2)固体混合物中硫酸镁的质量分数。_____(结果保留0.1%)
(3)恰好完全反应时,所得不饱和溶液中溶质的质量分数。_____
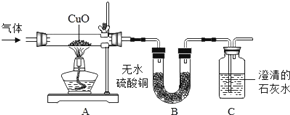
【题目】小明在实验室里进行以下实验:他首先取溶质质量分数为30%、密度为1.15gmL﹣1的较浓盐酸40mL与46g蒸馏水混合配制稀盐酸,再跟石灰石反应制得气体,将此气体通入澄清石灰水,但一直未见浑浊出现。为此,小明请教老师,老师建议他为弄明原因进行实验探究。下面是他探究的过程,请你帮他填答补充完整。
(提出问题)为什么制得的气体不能使石灰水变浑浊?
(猜想假设)猜想一:盐酸浓度仍过大,气体中有挥发出来的氯化氢气体
猜想二:澄清石灰水已经完全变质
(实验探究)
实验操作 | 实验现象 | 实验结论 |
①将所得气体通入稀硝酸和硝酸银的混合溶液中 | ______ | 猜想一正确 化学方程式______ |
②吸取少量所用澄清石灰水于试管中,滴加_____,振荡。 | 溶液变红色 | 猜想二不正确 |
(分析结论)原来所配盐酸浓度达_____,应当将其再进行稀释。
(反思拓展)①小明的实验证明了澄清石灰水没有完全变质,但是并不能说明澄清石灰水没有变质,理由是_____。
②若除掉二氧化碳中混有的少量氯化氢气体,可选择的最佳试剂是_____(填字母序号)。
a氢氧化钠溶液
b水
c饱和的碳酸氢钠溶液
d硝酸银溶液