题目内容
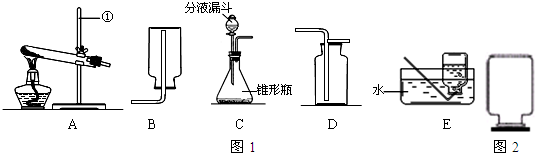
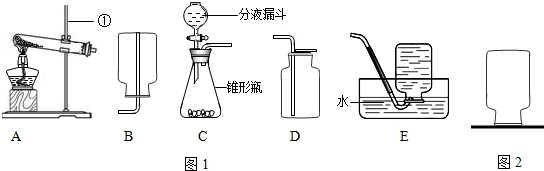
如图甲是实验室制取气体的一些装置,根据下图回答有关问题.(友情提示:以下所选装置均填装置标号)
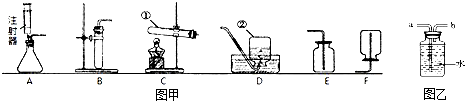
(1)写出序号为①②的仪器名称:①
(2)写出你知道的化学实验中可选用装置C制取气体的符号表达式
①该装置中试管口要略向下倾斜目的是
②收集所得气体可选用的装置是
③如果用排空气法收集氧气,如何验满?
(3)某学校化学兴趣小组在研究“带火星木条复燃与氧气体积分数的关系”的课题中,采取了以下实验步骤:
①取5只250mL集气瓶,分别装入25mL、50mL、75mL、100mL、125mL的水,并用毛玻璃片盖住,依次标号为1、2、3、4、5;
②用分解过氧化氢(H2O2)的方法制取氧气,用制取的氧气通过排水法将上述1~5号瓶中的水排去;
③将带火星的木条依次插入1~5号瓶中,把观察到观察和计算数据,填入下表.
试回答下列问题:
①实验室中采用分解过氧化氢(H2O2)的方法制取氧气,可采用的发生装置是(填标号)
②根据以上实验事实,下列说法中正确的是
A.只有在纯氧中才能使带火星的木条复燃
B.集气瓶中氧气的体积分数≥52.6%时,带火星的木条就能复燃
C.只要有氧气存在就可使带火星的木条复燃
(4)实验室在常温下用块状电石与水反应制取微溶于水的乙炔气体,该反应必须严格控制加水速度,以免剧烈反应放热引起发生装置炸裂.你认为上图中最适合制取乙炔气体的发生装置是

(1)写出序号为①②的仪器名称:①
试管
试管
;②集气瓶
集气瓶
.(2)写出你知道的化学实验中可选用装置C制取气体的符号表达式
2KClO3
2KCl+3O2↑
| ||
| △ |
2KClO3
2KCl+3O2↑
.
| ||
| △ |
①该装置中试管口要略向下倾斜目的是
防止冷凝水倒流引起试管炸裂
防止冷凝水倒流引起试管炸裂
;②收集所得气体可选用的装置是
D或E
D或E
;③如果用排空气法收集氧气,如何验满?
将带火星的木条放于集气瓶口,木条复燃则满
将带火星的木条放于集气瓶口,木条复燃则满
.(3)某学校化学兴趣小组在研究“带火星木条复燃与氧气体积分数的关系”的课题中,采取了以下实验步骤:
①取5只250mL集气瓶,分别装入25mL、50mL、75mL、100mL、125mL的水,并用毛玻璃片盖住,依次标号为1、2、3、4、5;
②用分解过氧化氢(H2O2)的方法制取氧气,用制取的氧气通过排水法将上述1~5号瓶中的水排去;
③将带火星的木条依次插入1~5号瓶中,把观察到观察和计算数据,填入下表.
| 集气瓶标号 | 1 | 2 | 3 | 4 | 5 |
| 集气瓶中氧气的体积分数 | 28.9% | 36.8% | 44.7% | 52.6% | 60.5% |
| 带火星木条的状况 | 微亮 | 亮 | 很亮 | 复燃 | 复燃 |
①实验室中采用分解过氧化氢(H2O2)的方法制取氧气,可采用的发生装置是(填标号)
A或B
A或B
,理由是过氧化氢溶液是液体,二氧化锰是固体,反应不需要加热
过氧化氢溶液是液体,二氧化锰是固体,反应不需要加热
;其反应的符号表达式是2H2O2
2H2O+O2↑
| ||
2H2O2
2H2O+O2↑
;该反应所属的基本反应类型是
| ||
分解反应
分解反应
.②根据以上实验事实,下列说法中正确的是
B
B
(填写相应的标号).A.只有在纯氧中才能使带火星的木条复燃
B.集气瓶中氧气的体积分数≥52.6%时,带火星的木条就能复燃
C.只要有氧气存在就可使带火星的木条复燃
(4)实验室在常温下用块状电石与水反应制取微溶于水的乙炔气体,该反应必须严格控制加水速度,以免剧烈反应放热引起发生装置炸裂.你认为上图中最适合制取乙炔气体的发生装置是
A
A
;如果用如图乙所示装置收集乙炔,气体应从b
b
(填“a”或“b”)端管口通入.分析:(1)识别一些简单仪器.
(2)装置C适用于加热固体制取气体,加热氯酸钾制取氧气可用此装置,并据氯酸钾分解的反应原理书写表达式;
①如果药品中有潮气,加热形成的水蒸汽到达试管口被冷却成水,水就会流向加热部位,导致试管爆裂,试管口向下就可避免这种情况;
②收集装置依据气体的溶解性和密度大小进行选择;
③检验氧气是否收集满是常见考点,方法是将带火星的木条放于集气瓶口观察现象进行判断;
(3)①发生装置的选择依据反应物的状态和反应的条件;并依据过氧化氢分解的反应原理书写表达式,依据反应特点判断反应类型;
②考查学生的分析识图能力,通过图表不难发现当氧气体积分数大于52.6%时,带火星的木条就能复燃;
(4)气体的发生装置和收集装置根据选择标准进行解答.
(2)装置C适用于加热固体制取气体,加热氯酸钾制取氧气可用此装置,并据氯酸钾分解的反应原理书写表达式;
①如果药品中有潮气,加热形成的水蒸汽到达试管口被冷却成水,水就会流向加热部位,导致试管爆裂,试管口向下就可避免这种情况;
②收集装置依据气体的溶解性和密度大小进行选择;
③检验氧气是否收集满是常见考点,方法是将带火星的木条放于集气瓶口观察现象进行判断;
(3)①发生装置的选择依据反应物的状态和反应的条件;并依据过氧化氢分解的反应原理书写表达式,依据反应特点判断反应类型;
②考查学生的分析识图能力,通过图表不难发现当氧气体积分数大于52.6%时,带火星的木条就能复燃;
(4)气体的发生装置和收集装置根据选择标准进行解答.
解答:解:(1)据常用仪器可知标号仪器分别是试管和集气瓶;
故答案为:试管;集气瓶;
(2)装置C适用于加热固体制取气体,加热氯酸钾制取氧气可用此装置,氯酸钾在加热、二氧化锰作催化剂的条件下生成氯化钾和氧气,反应的符号表达式是:2KClO3
2KCl+3O2↑;
故答案为:2KClO3
2KCl+3O2↑;
①如果药品中有潮气,加热时形成的水蒸气到达试管口被冷却成液态水;如果试管口朝上,就会流向加热部分,导致试管爆裂,所以试管口要略向下倾斜;
故答案为:防止冷凝水倒流引起试管炸裂;
②氧气不易溶于水,可以用排水法;密度比空气的密度大,可以采用向上排空气法;
故答案为:D或E
③用排空气法收集氧气验满的方法是:将带火星的木条放于集气瓶口,若木条复燃则满;
故答案为:将带火星的木条放于集气瓶口,木条复燃则满;
(3)①过氧化氢和二氧化锰制取氧气属于固体和液体不加热制氧气,故可选发生装置A或B;过氧化氢在二氧化锰的催化作用下生成水和氧气,反应的符号表达式是:
2H2O2
2H2O+O2↑;该反应由一种物质生成两种物质,属于分解反应;
故答案为:A或B;过氧化氢溶液是液体,二氧化锰是固体,反应不需要加热;2H2O2
2H2O+O2↑;分解反应;
②观察图表不难发现,当氧气体积分数大于52.6%时,带火星的木条就能复燃;
故选B;
(4)制取乙炔属于固体和液体不加热制取气体,要控制加水速度,可通过注射器实现,而B无法控制加水速度,故选发生装置A;由于乙炔不溶于水,从 b进入集气瓶,随着气体增多,迫使水从a出去进行收集气体;
故答案为:A;b.
故答案为:试管;集气瓶;
(2)装置C适用于加热固体制取气体,加热氯酸钾制取氧气可用此装置,氯酸钾在加热、二氧化锰作催化剂的条件下生成氯化钾和氧气,反应的符号表达式是:2KClO3
| ||
| △ |
故答案为:2KClO3
| ||
| △ |
①如果药品中有潮气,加热时形成的水蒸气到达试管口被冷却成液态水;如果试管口朝上,就会流向加热部分,导致试管爆裂,所以试管口要略向下倾斜;
故答案为:防止冷凝水倒流引起试管炸裂;
②氧气不易溶于水,可以用排水法;密度比空气的密度大,可以采用向上排空气法;
故答案为:D或E
③用排空气法收集氧气验满的方法是:将带火星的木条放于集气瓶口,若木条复燃则满;
故答案为:将带火星的木条放于集气瓶口,木条复燃则满;
(3)①过氧化氢和二氧化锰制取氧气属于固体和液体不加热制氧气,故可选发生装置A或B;过氧化氢在二氧化锰的催化作用下生成水和氧气,反应的符号表达式是:
2H2O2
| ||
故答案为:A或B;过氧化氢溶液是液体,二氧化锰是固体,反应不需要加热;2H2O2
| ||
②观察图表不难发现,当氧气体积分数大于52.6%时,带火星的木条就能复燃;
故选B;
(4)制取乙炔属于固体和液体不加热制取气体,要控制加水速度,可通过注射器实现,而B无法控制加水速度,故选发生装置A;由于乙炔不溶于水,从 b进入集气瓶,随着气体增多,迫使水从a出去进行收集气体;
故答案为:A;b.
点评:此题考查气体发生装置和收集装置的选择依据、反应原理、反应类型、气体的验满、实验注意事项等,同时也考查学生分析图表的能力,要灵活运用知识,达到举一反三的效果.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目