题目内容
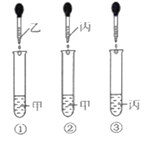
【题目】活泼金属可以和酸反应生成氢气,现在利用如图所示装置制取氢气,塑料片上放有足量锌粒,从漏斗中加入稀盐酸。
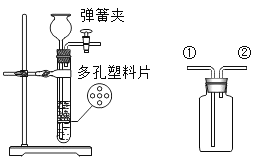
(1)该气体发生装置的优点是__________________,收集氢气可以从导管__________通入(填序号),点燃瓶中氢气前应进行的操作是____________________________________.
(2)锌粒和稀盐酸刚接触时没有气泡产生,过会才产生大量气泡其原因可能是_________________________.
(3)该气体发生装置一般不用于过氧化氢溶液和二氧化锰制氧气,其原因是__________________________,过氧化氢溶液和二氧化锰制氧气的化学方程式是____________________________________.
【答案】可控制反应开始和结束 ② 检验氢气纯度 表面有氧化物膜 二氧化锰是粉末状固体 ![]()
【解析】
(1)该装置可控制反应的发生与停止;氢气的密度比空气小,所以收集氢气可以从导管②进入;氢气具有可燃性,不纯时点燃可能会发生爆炸,所以点燃氢气前一定要检验氢气的纯度;
(2)锌的化学性质活泼,在空气中能与氧气反应生成氧化锌,锌粒刚放入稀盐酸中时,氧化锌与稀盐酸反应生成氯化锌和氢气,所以刚接触时没有气泡产生;
(3)二氧化锰是粉末状药品,所以不能用该装置来制取氧气,过氧化氢在二氧化锰的催化作用下生成氧气和水,化学方程式为:![]() 。
。

【题目】常见的盐的组成填表:
名称 | 化学式 | 阴离子 | 阳离子 |
氯化钠 | _____ | _____ | _____ |
碳酸钠 | _____ | _____ | _____ |
碳酸氢钠 | _____ | _____ | _____ |
碳酸钙 | _____ | _____ | _____ |
硫酸铜 | _____ | _____ | _____ |
【题目】为测定某样品(碳酸钠和氯化钠的混合物)中碳酸钠的质量分数,某化学兴趣小组进行以下实验,取50g的样品放置于气体发生装置中,然后取一定溶质质量分数的稀盐酸分5次加到该气体发生装置中,每次向装样品的烧杯中加入25g,实验测得加入稀盐酸的质量与实验时所得气体的质量的关系如下表。求:
加入稀盐酸的质量/g | 25 | 50 | 75 | 100 | 125 |
所得气体的质量/g | 4.4 | m | 4.4 | 4.4 | 0 |
(1)表中m的值为________。
(2)样品中碳酸钠的质量分数是________(精确到0.1%)。
(3)所用稀盐酸的溶质质量分数________(写出具体的计算过程)。