题目内容
【题目】请根据下列装置图,回答有关问题: 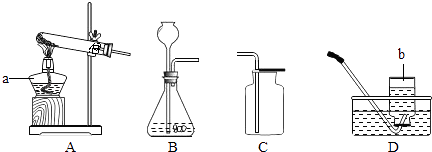
(1)写出装置图中标号仪器的名称:a , b .
(2)写出实验室用高锰酸钾制取氧气的化学方程式 , 可选用的发生装置是(填字母).
(3)写出实验室用锌粒与稀硫酸制取氢气的化学方程式 , 可选用的收集装置是(填字母).
(4)若要配置245g质量分数为10%的稀硫酸,需要质量分数为98%的浓硫酸(密度为1.84g/cm3)mL(计算结果保留一位小数),由浓溶液配制稀溶液时,计算的依据是 . 在实验室用浓硫酸配制稀硫酸的主要步骤有:计算、、混匀、冷却至室温装瓶并贴上标签.
【答案】
(1)酒精灯;集气瓶
(2)2KMnO4 ![]() K2MnO4+MnO2+O2↑;A
K2MnO4+MnO2+O2↑;A
(3)Zn+H2SO4═ZnSO4+H2↑;D
(4)13.6;溶液稀释前后,溶质的质量不变;量取
【解析】解:(1)标号仪器分别是酒精灯和集气瓶;(2)加热高锰酸钾生成锰酸钾、二氧化锰和氧气,方程式是:2KMnO4 ![]() K2MnO4+MnO2+O2↑,该反应需要加热,属于固体加热型,故选发生装置A;(3)锌和稀硫酸反应生成硫酸锌和氢气,方程式是:Zn+H2SO4═ZnSO4+H2↑,氢气的密度比空气小,应用向下排空气法收集,氢气难溶于水,所以还可用排水法收集;(4)根据配制前后溶液中的溶质质量不变,设需要98%浓硫酸溶液的体积为V,则有:245g×10%=98%×1.84g/cm3×V,解得V=13.6mL;在实验室用浓硫酸配制稀硫酸的主要步骤有:计算、量取浓硫酸和水,然后混匀、冷却至室温装瓶并贴上标签; 所以答案是:(1)酒精灯;集气瓶;(2)2KMnO4
K2MnO4+MnO2+O2↑,该反应需要加热,属于固体加热型,故选发生装置A;(3)锌和稀硫酸反应生成硫酸锌和氢气,方程式是:Zn+H2SO4═ZnSO4+H2↑,氢气的密度比空气小,应用向下排空气法收集,氢气难溶于水,所以还可用排水法收集;(4)根据配制前后溶液中的溶质质量不变,设需要98%浓硫酸溶液的体积为V,则有:245g×10%=98%×1.84g/cm3×V,解得V=13.6mL;在实验室用浓硫酸配制稀硫酸的主要步骤有:计算、量取浓硫酸和水,然后混匀、冷却至室温装瓶并贴上标签; 所以答案是:(1)酒精灯;集气瓶;(2)2KMnO4 ![]() K2MnO4+MnO2+O2↑;A;(3)Zn+H2SO4═ZnSO4+H2↑;D;(4)13.6;溶液稀释前后,溶质的质量不变;量取.
K2MnO4+MnO2+O2↑;A;(3)Zn+H2SO4═ZnSO4+H2↑;D;(4)13.6;溶液稀释前后,溶质的质量不变;量取.

 名校课堂系列答案
名校课堂系列答案【题目】在“人吸入的空气和呼出的气体有什么不同”的探究中,下列说法不正确的是( )
选项 | 现象 | 结论 |
A | 带火星木条不复燃 | 呼出气体中氧气含量低 |
B | 干燥玻璃片上有水雾 | 呼出气体中水含量高 |
C | 澄清石灰水变浑浊 | 呼出气体中二氧化碳含量高 |
D | 集气瓶正放 | 呼出气体的密度比空气大 |