题目内容
37、在生产和生活中,金属腐蚀所带来的损失非常严重,所以防止金属腐蚀已成为科学研究和技
术领域的重大问题.化学兴趣小组的同学在实验室中对金属的腐蚀进行了探究.
活动与探究一
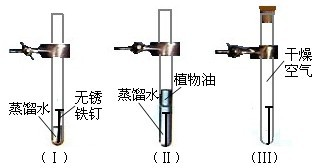
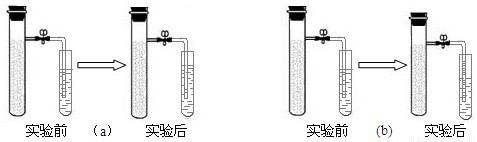
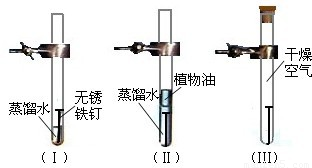
分别在三个洁净干燥的试管中各加一个洁净无锈的铁钉,再在其中两个试管中加入经煮沸迅速冷却的蒸馏水,其它操作请仔细观察下图:
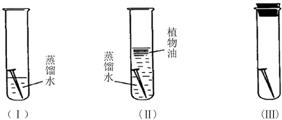
(1)探究结论:
活动与探究二
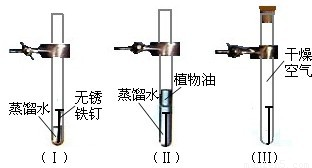
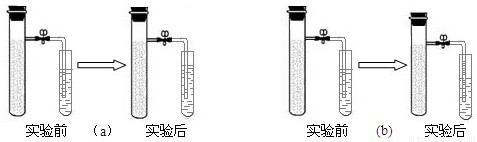
向铁粉中加入少量的炭粉(模拟铁钉的成分),混合均匀后,撒入内壁分别用稀盐酸和氯化钠溶液润湿过的两只具支试管(分别标记为a、b),按下图装好仪器.几分钟后,打开止水夹,观察发现:a装置右侧小试管中液面上升,导管中液面下降;而b装置右侧小试管中液面下降,导管中液面上升;b装置固体混合物中发现有红色物质生成.
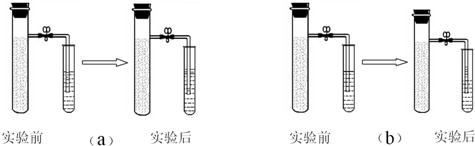
(2)请你推测:a装置右侧小试管中液面上升的原因是
(3)将“活动与探究一”中已生锈的铁钉放入稀盐酸中,可观察到
术领域的重大问题.化学兴趣小组的同学在实验室中对金属的腐蚀进行了探究.
活动与探究一
分别在三个洁净干燥的试管中各加一个洁净无锈的铁钉,再在其中两个试管中加入经煮沸迅速冷却的蒸馏水,其它操作请仔细观察下图:

(1)探究结论:
I
号试管中的铁钉最容易生锈.由此可见,铁制品生锈需要的条件是与氧气和水接触
.活动与探究二
向铁粉中加入少量的炭粉(模拟铁钉的成分),混合均匀后,撒入内壁分别用稀盐酸和氯化钠溶液润湿过的两只具支试管(分别标记为a、b),按下图装好仪器.几分钟后,打开止水夹,观察发现:a装置右侧小试管中液面上升,导管中液面下降;而b装置右侧小试管中液面下降,导管中液面上升;b装置固体混合物中发现有红色物质生成.

(2)请你推测:a装置右侧小试管中液面上升的原因是
有氢气产生
;b装置右侧小试管中液面下降的原因是氧气参加了反应
.(3)将“活动与探究一”中已生锈的铁钉放入稀盐酸中,可观察到
铁锈溶解
、溶液变黄
,化学方程式为Fe2O3+6HCl=2FeCl3+3H2O
.分析:(1)铁生锈的条件是:与氧气接触,有水参加.
(2)而单质铁可以和盐酸反应生成氢气,导致支管试管内气压增大排出导管内气体,致使图a中试管内液体上升.铁生锈消耗了氧气,导致支管试管内气压降低,致使图b中试管内液体下降.
(3)生锈的铁钉放入稀盐酸,先是铁锈溶解,后铁与盐酸反应.
(2)而单质铁可以和盐酸反应生成氢气,导致支管试管内气压增大排出导管内气体,致使图a中试管内液体上升.铁生锈消耗了氧气,导致支管试管内气压降低,致使图b中试管内液体下降.
(3)生锈的铁钉放入稀盐酸,先是铁锈溶解,后铁与盐酸反应.
解答:解:(1)铁生锈的条件是:与氧气接触,有水参加,二者缺一不可
(2)铁与盐酸反应生成了氢气,左侧试管中气体增加;而氧气与铁和水发生了反应会减少,左侧试管中气体减少.
(3)铁锈(Fe2O3)与盐酸反应而消失,溶液成黄色(Fe3+颜色)[如果进一步反应,铁与盐酸反应生成氢气,溶液呈浅绿色(Fe2+颜色)]
故答案为:(1)Ⅰ;铁与氧气、水接触;
(2)有氢气产生;氧气参加了反应.
(3)铁锈溶解;溶液变黄;Fe2O3+6HCl=2FeCl3+3H2O[铁锈溶解,并有气泡生成,溶液呈浅绿色,Fe2O3+6 HCl═2FeCl3+3 H2O和Fe+2 HCl═FeCl2+H2↑]
(2)铁与盐酸反应生成了氢气,左侧试管中气体增加;而氧气与铁和水发生了反应会减少,左侧试管中气体减少.
(3)铁锈(Fe2O3)与盐酸反应而消失,溶液成黄色(Fe3+颜色)[如果进一步反应,铁与盐酸反应生成氢气,溶液呈浅绿色(Fe2+颜色)]
故答案为:(1)Ⅰ;铁与氧气、水接触;
(2)有氢气产生;氧气参加了反应.
(3)铁锈溶解;溶液变黄;Fe2O3+6HCl=2FeCl3+3H2O[铁锈溶解,并有气泡生成,溶液呈浅绿色,Fe2O3+6 HCl═2FeCl3+3 H2O和Fe+2 HCl═FeCl2+H2↑]
点评:铁生锈的条件是氧气和水都与铁接触,酸与铁反应生成氢气,氯化钠能促进铁的锈蚀.生锈的铁钉与酸反应,一般只考虑第一步,第二步反应一般不予考虑.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
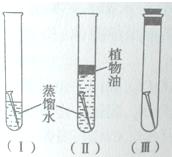 〔活动与探究一〕
〔活动与探究一〕