题目内容
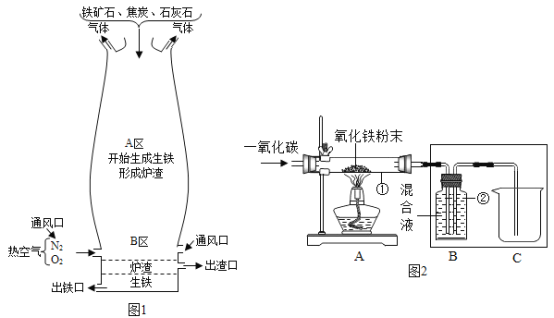
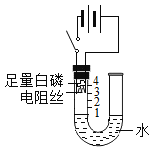
【题目】根据如图所示实验回答下列问题:
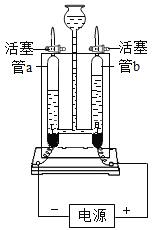
(1)接通直流电源一段时间后,玻璃管a内产生的气体是_____。
(2)检验管b气体的方法是_____。
(3)若将管a与管b上的活塞全打开,管a与管b中的液面将_____。
【答案】氢气 将带火星的木条放在管b尖嘴处,木条复燃,说明是氧气 相平
【解析】
(1)电解水时,与电源正极相连的试管内产生的气体体积少,是氧气,与电源负极相连的试管内的气体体积多,是氢气,且两者的体积之比大约是1:2,故a内产生的是氢气。
(2)管b气体是氧气,进行分析解答。
(3)将管a与管b上的活塞全打开,生成的气体逸出,两管内压强相等,进行分析解答。
(1)电解水时,与电源负极相连的试管内的气体体积多,玻璃管a内产生的气体是氢气。
(2)管b气体是氧气,氧气能支持燃烧,可将带火星的木条放在管b尖嘴处,木条复燃,说明是氧气。
(3)将管a与管b上的活塞全打开,生成的气体逸出,两管内压强相等,管a与管b中的液面将相平。
故答案为:
(1)氢气;
(2)将带火星的木条放在管b尖嘴处,木条复燃,说明是氧气;
(3)相平。

【题目】钠是一种活泼金属,常温下能与氧气、水等物质发生反应。钠与水反应的化学方程式为:2Na+2H2O==2NaOH+H2↑。在实验室,小亮先取定量的硫酸铜溶液于烧杯中,再取一小块钠投入硫酸铜溶液中,充分反应后过滤,得到滤液和蓝色滤渣,并对滤被的成分进行探究。
(提出问题)滤液中溶质的成分是什么?
(查阅资料)Na2SO4溶液呈中性
(猜想与假设)猜想一:Na2SO4
猜想二:Na2SO4和NaOH
猜想三:____________
猜想四:Na2SO4、CuSO4和NaOH
小明认为猜想______不合理,理由是_______(用化学方程式表示)。
(实验与验证)
实验 | 实验操作 | 实验現象 | 实验结论 |
实验一 | 取少量滤液于试管中,仔细观察现象 | 溶液为无色 | 猜想_____不成立 |
实验二 | 向实验一所取滤液中滴入酚酞溶液 | ________ | 猜想二不成立 |
实验三 | 常温下,再取少量滤液,测溶液酸碱度 | pH=7 | 猜想_____成立 |
(拓展延伸)金属活动性顺序表中钠及前面的金属____(填“能”或“不能”)把位于后面的金属从它们盐溶液里置换出来。