题目内容
【题目】碳是形成化合物种类最多的元素,含碳物质是中学化学研究的重要内容.
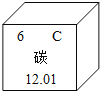
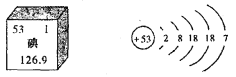
(1)如图为元素周期表中的一格,下列说法不正确的是______.
A.碳元素属于非金属元素
B.碳原子核内质子数为6
C.碳元素的原子结构示意图为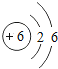
D.碳的相对原子质量为12.01
(2)“低碳生活”倡导低能耗、低污染、低排放,主要是为了减少______(填化学式)的排放量.下列做法符合“低碳经济”的是______.
①提倡发送电子贺卡②大力发展火力发电③研制和开发新能源④提倡使用一次性木筷⑤增强室内自然采光
(3)二氧化碳和氨气(NH3)在高温、高压下反应,生成尿素[CO(NH2)2]和水,反应的化学方程式是______.
【答案】C CO2 ①③⑤ CO2+2NH3![]() CO(NH2)2+H2O
CO(NH2)2+H2O
【解析】
(1)A、因碳的偏旁为“石”,则碳元素为非金属元素,故A正确;B、由信息可知,碳原子的质子数为6,故B正确;C、碳原子的质子数为6,则原子结构中最外层电子数应为4,故C错误;D、由信息可知,碳原子的相对原子质量为12.01,故D正确;故选C.
(2)“低碳生活”倡导低能量、低消耗,主要是为了减少二氧化碳的排放,通过技术创新、制度创新、产业转型、新能源开发等多种手段,尽可能地减少煤炭、石油等高碳能源消耗,减少温室气体排放,达到经济、社会发展与生态环境保护双赢的一种经济发展形态,属于低碳经济.①提倡发送电子贺卡、③研制和开发新能源、⑤增强室内自然采光都可减少二氧化碳的排放,而②大力发展火力发电需要燃烧煤,增加二氧化碳的排放;④提倡使用一次性木筷必然要砍伐木材,减少了自然界对二氧化碳的吸收.
(3)二氧化碳和氨气(NH3)在高温、高压下反应,生成尿素[CO(NH2)2]和水,反应的化学方程式是CO2+2NH3![]() CO(NH2)2+H2O.
CO(NH2)2+H2O.

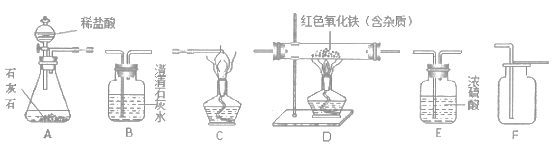
【题目】硫酸(H2SO4)是一种用途广泛的化工原料,工业上常用煅烧黄铁矿(主要成分是FeS2)的方法来生产硫酸,简要的工艺流程图如下:
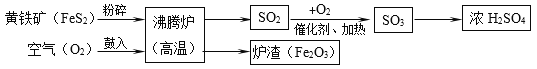
(1)黄铁矿投入沸腾炉前粉碎的目的是________。
(2)在沸腾炉中发生的反应为:(______)FeS2+(______)O2 ![]() (______)Fe2O3+(______)SO2(请在化学式前面配上适当的化学计量数),得到的炉渣(Fe2O3)可用来炼铁。
(______)Fe2O3+(______)SO2(请在化学式前面配上适当的化学计量数),得到的炉渣(Fe2O3)可用来炼铁。
(3)请写出流程中SO2转化为SO3的化学方程式_________。
(炉渣的综合利用)
为了实现炉渣(Fe2O3)的综合利用,工业上把炉渣和焦炭、石灰石一起投入高炉,主要反应过程如图:
![]()
(4)步骤②发生反应的化学方程式为______。
(5)下列有关高炉炼铁的说法正确的是_______(填序号)。
A.上述流程中涉及的三个反应均为吸热反应
B.上述步骤①反应中,还原剂是焦炭
C.焦炭的作用之一是为炼铁炉提供高温条件
D.焦炭的另一个作用是除去铁矿石中的杂质
(6)分析高炉所得的生铁中单质铁的含量:
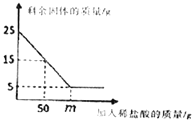
小瑾同学为测定生铁中铁的质量分数,先后进行了四次实验,实验数据记录如下表。根据她的实验数据,试计算生铁中铁的质量分数是_________?
第一次 | 第二次 | 第三次 | 第四次 | |
所取生铁的质量∕g | 10 | 10 | 10 | 10 |
所加稀硫酸的质量∕g | 25 | 50 | 75 | 100 |
生成氢气的质量∕g | 0.10 | 0.20 | 0.30 | 0.35 |
(反思质疑)
小宇同学在梳理工业炼铁的相关知识时,提出了以下质疑:
(质疑一)焦炭也具有还原性而且成本低,工业炼铁为什么不直接用焦炭作为还原剂冶炼铁矿石?
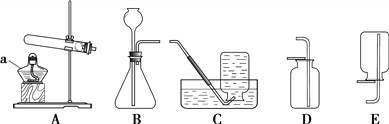
(7)他设计了下图所示的一组对比实验:称取两份相同质量的氧化铁粉末,一份与足量的焦炭粉末混合均匀放入装置A的试管中,另一份放入装置B的玻璃管中。
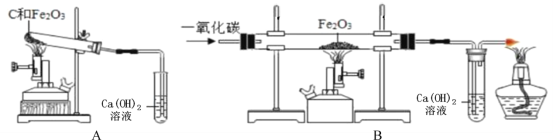
①装置B的玻璃管中发生反应的化学方程式为________。
②当他观察到装置B的玻璃管中固体_________、澄清石灰水变浑浊时,装置A
③通过上述实验对比,小宇同学认为工业上不直接用焦炭作为还原剂炼铁的主要原因有:反应不充分、反应速度慢、_______等。
(质疑二)装置B中反应后的黑色固体一定就是单质铁吗?
(查阅资料)
a.铁常见的氧化物有氧化铁(Fe2O3)、四氧化三铁(Fe3O4)和氧化亚铁(FeO)。
b.四氧化三铁是具有磁性的黑色晶体,氧化亚铁是不溶于水的黑色粉末,无磁性,也不能被磁铁吸引。
④小宇同学设计了如下实验方案:用磁铁吸引装置B进行实验后的黑色固体,发现黑色固体可以部分被吸引,由此得出结论:黑色固体的成分是___________。