题目内容
【题目】氧化镁常与氢氧化铝合用,主要用于治疗伴有便秘的胃酸过多症、胃及十二指肠溃疡,还可用作缓泻剂。以镁矿石(主要成分为MgCO3 ,SiO2 )为原料生产MgO的工艺流程如下:
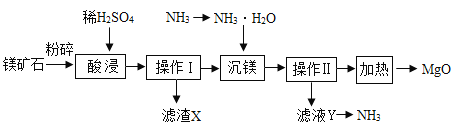
资料:SiO2难溶于水和常见的酸。
(1)粉碎镁矿石的目的是_________________。
(2)操作I的名称为_________________。
(3)酸浸的目的是_________________。
(4)“沉镁”时,MgSO4与NH3﹒H2O发生反应生成Mg(OH)2 ,写出该反应的化学方程式:_________________。
【答案】增大反应物之间的接触面积,使反应更充分 过滤 把不溶于水的碳酸镁转化为溶于水的硫酸镁 ![]()
【解析】
(1)粉碎镁矿石的目的是增大反应物之间的接触面积,使反应更充分。故填:增大反应物之间的接触面积,使反应更充分。
(2)操作I得到的是滤渣和滤液,是过滤操作,故填:过滤;
(3)稀硫酸能与碳酸镁反应生成硫酸镁、水和二氧化碳 ,所以酸浸的目的是把不溶于水的碳酸镁转化为溶于水的硫酸镁。故填:把不溶于水的碳酸镁转化为溶于水的硫酸镁;
(4)根据复分解反应的规律,“沉镁”时,MgSO4与NH3﹒H2O发生反应交换成分生成Mg(OH)2 和硫酸铵,该反应的化学方程式为:![]() 。故填:
。故填:![]() 。
。

【题目】(8分)目前市场上的补钙药剂很多,下图是某品牌补钙药品的部分说明书.

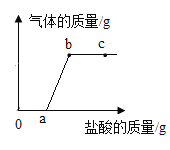
为测定其含量是否达标,某兴趣小组的同学取10片钙片研碎后放于烧杯中,将100g稀盐酸分五次加入到烧杯中,并不断搅拌,称量,将得到的有关数据记录如下(钙片中其它成分不与稀盐酸反应):
加入稀盐酸的质量/g | 0 | 20 | 40 | 60 | 80 | 100 |
烧杯中剩余物质质量/g | 10 | 29.12 | 48.24 | 67.36 | 86.48 | 106.48 |
请你根据题给信息和表中数据,回答下列问题:
(1)实验过程中将钙片研碎的目的是: .
(2)完全反应后,产生二氧化碳的质量为 g.
(3)试通过计算说明,该品牌钙片含量是否达标.(写出计算过程)
(4)如果按用量服用,服用者每天通过该补钙剂摄入钙元素的质量为 g.