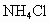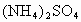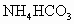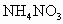题目内容
为了鉴定某种肥料晶体,进行下列实验:①看外观,白色晶体;
②取少量晶体与熟石灰混合,加热混合物,闻到刺激性气味;
③将少量晶体投入稀盐酸,晶体溶解,没有气体产生;
④将少量晶体溶于水,再加入氯化钡溶液,生成白色沉淀,再加入稀硝酸,白色沉淀不溶解.
(1)根据上述实验判断,肥料晶体是______
A.NH4Cl
B.(NH4)2SO4
C.NH4HCO3
D.NH4NO3
(2)某同学为了证明某白色晶体是(NH4)2SO4,他设计了两点程序:第一步,为了证明铵根离子的存在,必需的操作步骤是______.当观察到______现象时,证明有铵根离子存在.第二步,为了证明硫酸根离子的存在,该学生设计了三种方案:①加入氯化钡溶液再加稀盐酸;②加入过量盐酸酸化了的BaCl2溶液;③先加过量的盐酸酸化,再加氯化钡溶液.你认为上述三种方案中最合理的一种方案是______,简述理由______.
(3)另有一同学为确定一种化肥样品的成分,进行如下实验:①取少量样品放入试管中,加入3mL氢氧化钠溶液,在酒精灯上微热,把湿润的红色石蕊试纸放在试管口,试纸变蓝.②另取少量样品于试管中,加入少量水,溶解,滴入几滴硝酸钡溶液,有白色沉淀生成,加入足量稀硝酸,沉淀不溶解.由以上实验可以判断此化肥是______(写化学式).
【答案】分析:(1)与熟石灰混合,加热能产生有刺激性气味的气体是氨气,说明该物质含有铵根;与盐酸混合没有气体生成,说明物质中没有碳酸根离子或碳酸氢根离子;不溶于硝酸的沉淀有硫酸钡沉淀或氯化银沉淀;(2)铵盐遇见碱放氨气;硫酸钡是不溶于稀硝酸的白色沉淀;(3)与碱反应生成湿润的红色石蕊试纸放在试管口,试纸变蓝,说明产生的氨气;不溶于硝酸的白色沉淀有硫酸钡沉淀和氯化银沉淀,再进行分析.
解答:解:(1)晶体与熟石灰混合,加热能产生有刺激性气味的气体是氨气,说明该物质含有铵根;与盐酸混合没有气体生成,说明物质中没有碳酸根离子或碳酸氢根离子,故C错;将少量晶体溶于水,再加入氯化钡溶液,生成白色沉淀,再加入稀硝酸,白色沉淀不溶解,不溶于硝酸的沉淀有硫酸钡沉淀或氯化银沉淀,由于所提供的物质中没有银离子,所以不溶于硝酸的白色沉淀是硫酸钡沉淀,所以该物质中含有硫酸根,所以肥料是硫酸铵,故选B;
(2)铵根离子的检验通常是加入碱,然后观察是否有刺激性气体产生,故答案为:加入熟石灰混合研磨;有刺激性气味的气体冒出;先加过量盐酸酸化,以除去银离子的干扰,然后再加BaCl2溶液.如产生不溶于稀硝酸的白色沉淀,则证明含有硫酸根;故答案为:③;排除了Ag+的干扰;
(3)与碱反应生成湿润的红色石蕊试纸放在试管口,试纸变蓝,说明产生的是显碱性的氨气,说明该化肥中含有铵根离子;不溶于硝酸的白色沉淀有硫酸钡沉淀和氯化银沉淀,由于滴入几滴硝酸钡溶液,有白色沉淀生成,加入足量稀硝酸,沉淀不溶解,因为该化肥中含有铵根离子,没有银离子,所以该白色沉淀只能是硫酸钡沉淀,所以该化肥中含有硫酸根离子,所以化肥是硫酸铵,化学式是:(NH4)2SO4.
故答案为:(1)B;(2)加入熟石灰混合研磨;有刺激性气味的气体冒出;③;排除了Ag+的干扰;(3)(NH4)2SO4.
点评:本题主要考查了离子的检验,难度不大,根据离子的组成确定盐的成分,需要掌握铵根离子和硫酸根离子的检验方法.
解答:解:(1)晶体与熟石灰混合,加热能产生有刺激性气味的气体是氨气,说明该物质含有铵根;与盐酸混合没有气体生成,说明物质中没有碳酸根离子或碳酸氢根离子,故C错;将少量晶体溶于水,再加入氯化钡溶液,生成白色沉淀,再加入稀硝酸,白色沉淀不溶解,不溶于硝酸的沉淀有硫酸钡沉淀或氯化银沉淀,由于所提供的物质中没有银离子,所以不溶于硝酸的白色沉淀是硫酸钡沉淀,所以该物质中含有硫酸根,所以肥料是硫酸铵,故选B;
(2)铵根离子的检验通常是加入碱,然后观察是否有刺激性气体产生,故答案为:加入熟石灰混合研磨;有刺激性气味的气体冒出;先加过量盐酸酸化,以除去银离子的干扰,然后再加BaCl2溶液.如产生不溶于稀硝酸的白色沉淀,则证明含有硫酸根;故答案为:③;排除了Ag+的干扰;
(3)与碱反应生成湿润的红色石蕊试纸放在试管口,试纸变蓝,说明产生的是显碱性的氨气,说明该化肥中含有铵根离子;不溶于硝酸的白色沉淀有硫酸钡沉淀和氯化银沉淀,由于滴入几滴硝酸钡溶液,有白色沉淀生成,加入足量稀硝酸,沉淀不溶解,因为该化肥中含有铵根离子,没有银离子,所以该白色沉淀只能是硫酸钡沉淀,所以该化肥中含有硫酸根离子,所以化肥是硫酸铵,化学式是:(NH4)2SO4.
故答案为:(1)B;(2)加入熟石灰混合研磨;有刺激性气味的气体冒出;③;排除了Ag+的干扰;(3)(NH4)2SO4.
点评:本题主要考查了离子的检验,难度不大,根据离子的组成确定盐的成分,需要掌握铵根离子和硫酸根离子的检验方法.

练习册系列答案
相关题目
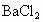 溶液,生成白色沉淀;再加入稀硝酸,沉淀不溶解.
溶液,生成白色沉淀;再加入稀硝酸,沉淀不溶解.