题目内容
某课外小组欲测定某石灰石样品中碳酸钙的质量分数,进行了以下实验:
①称取该样品10g;
②加入足量的稀盐酸充分反应(样品中杂质不与盐酸反应);
③将所生成的全部气体除杂干燥后,通入100g氢氧化钠浓溶液,反应后称得此溶液总质量为102.2g。 请计算:该石灰石样品中碳酸钙的质量分数是多少?
①称取该样品10g;
②加入足量的稀盐酸充分反应(样品中杂质不与盐酸反应);
③将所生成的全部气体除杂干燥后,通入100g氢氧化钠浓溶液,反应后称得此溶液总质量为102.2g。 请计算:该石灰石样品中碳酸钙的质量分数是多少?
解:
设样品中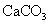 的质量为x
的质量为x

100 44
x 2.2g


样品中:
答:样品中碳酸钙的质量分数是50%。

设样品中
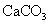 的质量为x
的质量为x
100 44
x 2.2g


样品中:

答:样品中碳酸钙的质量分数是50%。

练习册系列答案
 小学课时特训系列答案
小学课时特训系列答案
相关题目
某实验小组欲测定某白色粉末(已知是碳酸钠与碳酸氢钠的混合物)的组成,取三份质量不同的样品甲、乙、丙分别与30g稀盐酸充分反应,得到的常温常压下气体体积关系如下表,试求:
(1)样品中碳酸钠的质量分数?
(2)稀盐酸的质量分数?(已知二氧化碳常温常压下的密度是1.97g/L)(计算过程中保留两位小数)
(1)样品中碳酸钠的质量分数?
(2)稀盐酸的质量分数?(已知二氧化碳常温常压下的密度是1.97g/L)(计算过程中保留两位小数)
| 甲 | 乙 | 丙 | 混合物质量/g | 3.80 | 7.60 | 11.4 | 二氧化碳的体积/L | 0.893 | 1.786 | 1.786 |