题目内容
7.请根据下列图示回答问题:①甲图中R物质在室温(20℃)时的饱和状态为D点,40℃时的饱和状态为A点,现将 甲图中的R溶液从A状态变到B状态,请设计并简述一个简单的实验操作途径:可先将R溶液从A状态稀释到C状态,再将温度升高到60℃.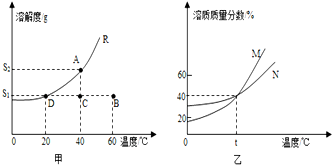
②乙图是表示M、N两种物质饱和溶液的溶质质量分数随温度变化的曲线.现分别向60g M、80g N固体中各加入150g水,并加热至完全溶解,同时各蒸发掉50g水,冷却至t℃,下列分析正确的是ae(填序号,多选、少选、错选均不给分). a.只有N析出晶体; b.M、N两种溶液的溶质质量分数相等; c.只有M析出晶体:d.M、N均有晶体析出:e.M、N两种物质的溶解度相同.
分析 (1)根据饱和溶液与不饱和溶液可通过改变温度、增减溶剂或溶质的方法实现互相转化,溶液状态的变化就使得曲线图中的点做相应地移动进行分析;
(2)根据题意,加水150克,加热溶解,同时蒸发掉50克水,冷却至T℃,这一系列变化后,相当于在T℃时用150g-50g=100g水分别去溶解50克M和80克N固体,判断此时的溶解情况;因此可根据饱和溶液的溶质质量分数随温度变化的曲线,算出T℃两物质的溶解度,然后判断此时100g水所能溶解两种物质的最大值,从而对所做的判断进行评价.
解答 解:(1)从溶液状态分析,A溶液为低温时饱和溶液,B溶液为高温时的不饱和溶液,可先将R溶液从A状态稀释到C状态,再将温度升高到60℃;也可先将A状态的R溶液温度降低到20℃,过滤后再将滤液温度升高到60℃.A状态由两种不同途径变到B状态时,两种途径都达到了相同的饱和程度,因此溶质质量分数相等;
故答案为:可先将R溶液从A状态稀释到C状态,再将温度升高到60℃;
(2)首先计算T℃时M、N两物质的溶解度:根据饱和溶液的溶质质量分数随温度变化的曲线,T℃时M、N两物质的饱和溶液的溶质质量分数相等都为40%,根据饱和溶液的溶质质量分数与溶解度的关系,可知此时两物质的溶解度相等,都为
| 40% |
| 1-40% |
然后根据溶解度判断两物质在T℃时的溶解情况:T℃时M、N两物质的溶解度为67g,即此时100g水最多溶解M、N物质的质量都为67g,所以,加入的50gM可以全部溶解且形成不饱和溶液,加入的80gN不能全部溶解而成为饱和溶液;
综合以上分析,当降温到T℃时固体M不会析出,而固体N物质析出80g-67g=13g;由于此时M溶液不饱和溶液而N溶液为饱和溶液,因此两溶液的溶质质量分数也不相等;此温度下M、N两种物质的溶解度相同.
故ae正确,bcd不正确.
故答案为:(1)可先将R溶液从A状态稀释到C状态,再将温度升高到60℃;
(2)ae.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.有X、Y、Z三种溶液,进行如图实验,则X、Y、Z依次可能是( )
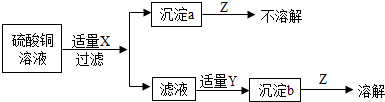

| A. | NaOH、BaCl2、稀HNO3 | B. | Ba(0H)2、AgNO3、稀盐酸 | ||
| C. | BaCl2、NaOH、稀HNO3 | D. | BaCl2、AgNO3、稀HNO3 |
20.下列有关纯碱的说法正确的是( )
| A. | 纯碱难溶于水 | |
| B. | 纯碱就是纯度比较高的碱 | |
| C. | 纯碱中含有少量的小苏打可以用稀盐酸除去 | |
| D. | 纯碱既可以从内陆盐湖提取,又可用“侯氏联合制碱法”生产 |
17.由+2价的X和-1价的Y两种元素组成的化合物的化学式为( )
| A. | XY2 | B. | X2Y | C. | YX2 | D. | Y2X |
12.物质加入足量水能得到悬浊液的是( )
| A. | 冰糖 | B. | 味精 | C. | 泥沙 | D. | 食盐 |
19.鉴别下列各组物质,所选用的试剂正确的是C
| 被鉴别的物质 | 选用试剂 | |
| A | 氢氧化钠溶液和澄清石灰水 | 稀盐酸 |
| B | 氯化钠溶液和稀盐酸 | 无色酚酞 |
| C | 硝酸铵固体和氢氧化钠固体 | 水 |
| D | 氯化钾固体与硫酸铵固体 | 氢氧化钙 |
17.现有氧化镁和氧化铁组成的混合物共10g,放入100g稀盐酸中充分反应后,测得共生成水3.6g,则稀盐酸溶质的质量分数最小为( )
| A. | 7.3% | B. | 14.6% | C. | 36% | D. | 40% |