题目内容
【题目】根据以下题图回答有关问题:
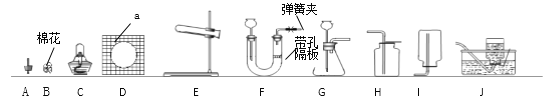
(1)仪器a的名称是__________。
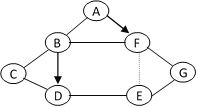
(2)实验室用KMnO4制备O2应选用的装置用品是________(填序号,下同),反应的化学方程式是_____。若用装置J收集氧气,当气体收集完毕时,应先_______。A.从水中取出导气管 B.熄灭酒精灯
(3)制备氢气能使反应随时发生或停止应选用的装置是_________,发生反应的化学方程式为_______,收集装置应选____________。
(4)实验室制备Cl2的原理是: MnO2 + 4HCl(浓)![]() MnCl2 + Cl2↑ + 2H2O,制备Cl2应选用的装置是(夹持装置略去)________,Cl2能溶于水,密度比空气大,收集Cl2应选用的装置是__________。
MnCl2 + Cl2↑ + 2H2O,制备Cl2应选用的装置是(夹持装置略去)________,Cl2能溶于水,密度比空气大,收集Cl2应选用的装置是__________。
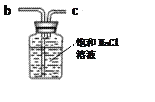
(5)若用下图装置收集Cl2,气体应从______口进入
【答案】 石棉网 ABCEH或ABCEJ 2KMnO4![]() K2MnO4 + MnO2 + O2↑ A F Zn + H2SO4 = ZnSO4 + H2↑ I或J CDG H c
K2MnO4 + MnO2 + O2↑ A F Zn + H2SO4 = ZnSO4 + H2↑ I或J CDG H c
【解析】本考点主要考查了气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写等,综合性比较强。气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关。
(1)仪器a的名称是石棉网;
(2)加热高锰酸钾制取氧气的装置,属于固—固加热型,氧气的密度大于氧气,可用向上排空气制取,氧气不易溶于,可用排水法收集,实验室用KMnO4制备O2应选用的装置用品是ABCEH或ABCEJ;高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,反应的化学方程式是2KMnO4![]() K2MnO4 + MnO2 + O2↑;若用装置J收集氧气,当气体收集完毕时,为了防止水倒流,应先从水中取出导气管,故选A;
K2MnO4 + MnO2 + O2↑;若用装置J收集氧气,当气体收集完毕时,为了防止水倒流,应先从水中取出导气管,故选A;
(3)将锌放在带孔隔板上,硫酸溶液通过长颈漏斗加入,打开弹簧夹,液体流下与锌接触,产生气体,关闭弹簧夹,容器内的压强增大,液面下降,硫酸溶液与锌脱离接触,反应停止。制备氢气能使反应随时发生或停止应选用的装置是F,锌与硫酸反应生成硫酸锌和氢气,发生反应的化学方程式为Zn + H2SO4 = ZnSO4 + H2↑,氢气难溶于水,可用排水法收集,氢气的密度小于空气,可用向上排空气法收集,收集装置应选I或J;
(4)根据实验室制备Cl2的原理可知,制备Cl2是用固体与液体混合加热,制备Cl2应选用的装置是CDG (夹持装置略去),Cl2能溶于水,密度比空气大,可用向上排空气法收集,收集Cl2应选用的装置应是H;
(5)Cl2的密度小于饱和食盐水,若用下图装置收集Cl2,气体应从C口进入。

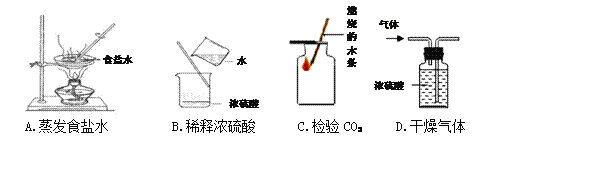
【题目】某同学进行如图两个实验。
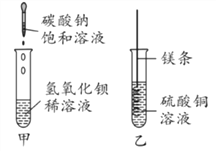
(1)甲实验中反应的化学方程式为________________________________。
(2)乙实验观察到的现象是__________________,溶液由蓝色变成无色。
(3)把甲、乙反应后的溶液倒入同一烧杯,发现有白色沉淀生成。他决定对白色沉淀的成分进行探究。
(查阅资料)硫酸钡不溶于酸。
(提出猜想)白色沉淀为:Ⅰ.________;
Ⅱ.Mg(OH)2和BaSO4;
Ⅲ.Mg(OH)2和MgCO3。
(实验方案)
实验操作 | 实验现象与结论 |
过滤、洗涤白色沉淀备用;向白色沉淀加入盐酸至过量 | ①若沉淀全部溶解,且无其它现象;猜想Ⅰ成立;其化学反应方程式为__________________。 ②若________________且无气体产生,猜想Ⅱ成立。 ③若沉淀完全溶解,____________,猜想Ⅲ成立。 |
(反思评价)如果猜想Ⅲ成立,产生此结果的原因是做甲实验时________________;上述白色沉淀的成分不可能出现的组合是Mg(OH)2、MgCO3和BaSO4,原因是:_________________。