题目内容
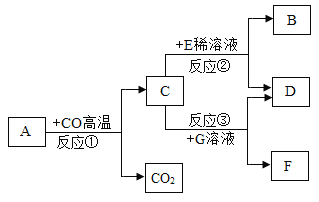
【题目】如图所示,A-J为初中化学中常见的物质。已知A为氧化物,组成元素的质量比为5:2,D为蓝色沉淀,F溶液为浅绿色。“→”表示物质间存在着相互转化的关系(部分生成物未标出)如图所示。请回答下列问题。

(1)E的化学式为_______;其用途是_____(任写一种)。
(2)B转化为D的化学方程式_________。其基本反应类型是______。B与I反应的化学方程式_____。A转化为B的实验现象是______。
【答案】CuSO4 用于湿法炼铜(或作杀菌剂、制波尔多液) Ca(OH)2+CuSO4=Cu(OH)2↓+CaSO4(合理即可) 复分解反应 ![]() 固体溶解,放出热量
固体溶解,放出热量
【解析】
A~J为初中化学中常见的物质,D为蓝色沉淀,所以D是氢氧化铜沉淀,E和氢氧化钠反应生成氢氧化铜沉淀,所以E可以是硫酸铜,F为浅绿色溶液,所以H是铁,铁和硫酸铜反应生成硫酸亚铁和铜,所以G是铜,F是硫酸亚铁,A为氧化物,组成元素的质量比为5:2,所以A是氧化钙,氧化钙和水反应生成氢氧化钙,氢氧化钙会与I反应生成和氢氧化钠,所以B是氢氧化钙,I是碳酸钠,C是碳酸钙;J是硫酸铜与硝酸钡反应生成的硫酸钡或硝酸铜;经过验证,推断正确。
(1)由分析可知,E的化学式为CuSO4,其用途是用于湿法炼铜(或作杀菌剂、制波尔多液);
(2)B转化为D的反应是氢氧化钙和硫酸铜反应生成氢氧化铜沉淀和硫酸钙,化学方程式为:Ca(OH)2+CuSO4=Cu(OH)2↓+CaSO4,基本反应类型是复分解反应;
B与I的反应是氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,化学方程式为:Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;
A转化为B的反应是氧化钙和水反应生成氢氧化钙,实验现象是:固体溶解,放出热量。

【题目】某化学兴趣小组在学习酸碱中和反应实验时,进行了如下探究:
I探究酸和碱能否发生反应
甲同学向盛有少量KOH溶液的试管中滴入几滴无色酚酞试液,振荡,继续加入稀盐酸,观察到溶液由_______色变成无色。甲同学得出结论:酸和碱能发生反应。
请写出稀盐酸和氢氧化钾溶液反应的化学方程式_____________。
Ⅱ探究酸和碱反应后溶液中溶质的成分
乙同学对探究I中甲同学实验后的无色溶液展开探究
(提出问题)试管中无色溶液的溶质除了酚酞还有什么?
(提出猜想)(1)KCl;(2)KCl和__________(填化学式)。
(设计实验)
方案 | 实验操作 | 实验现象及方程式 | 实验结论 |
方案1 | 试管中加入少量碳酸钠,然后加入过量甲同学实验后的无色溶液 | 可观察到溶液中有_______产生,化学反应方程式为________。 | 猜想(2)成立 |
方案2 | 用玻璃棒蘸取少量反应后的溶液滴在PH试纸上 | pH________7(填“>“<”或“=”) | |
方案3 | 取少量实验后的无色溶液于试管中,然后慢慢加NaOH溶液,并不断振荡试管 | 开始无明显现象,过一会发现_______。 |
(发散思维)
为了验证猜想(2)成立,你认为还可以选择的物质是_________(填选项)。
A二氧化碳 B锌粒 C氧化铜 D紫色石蕊试液
【题目】(1)定性检测(已知:无水CuSO4遇水变蓝色)
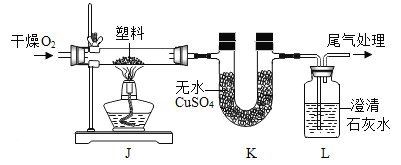
实验操作 | 实验现象 | 结论 |
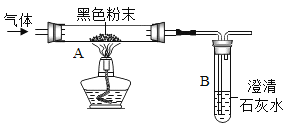
连接上图所示装置,_____,装入试剂,一段时间后,点燃J处酒精灯。 | 装置K中无水CuSO4_____色; | 塑料燃烧产物中有H2O |
装置L中澄清石灰水变浑浊。 | 塑料燃烧产物中有_____ |
由上述实验可知,该塑料一定含有的元素是_____(填元素符)。
(2)定量测定
为进一步确定组成,将2.8g该塑料在足量O2中完全燃烧,共产生了8.8gCO2和3.6gH2O,依据质量守恒定律,可判断该塑料_____(填“含有”或“不含”)除上述④中结论之外的元素。
【题目】人类的生产生活离不开金属材料
(1)人类历史上金属大规模开发、利用的先后顺序与多种因素有关,请列举一条相关的因素_____。
(2)下表示一些金属的熔点数据:
金属 | 铅 | 锡 |
熔点/℃ | 327.5 | 231.9 |
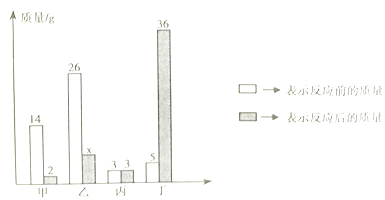
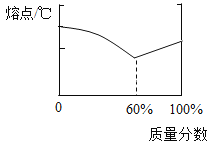
锡铅合金中某种金属的质量分数与合金熔点有如图所示的关系。当合金熔点最低时,合金中锡与铅的质量比是_____。
(3)如下图所示,为实验室中常见的气体制取和收集装置:
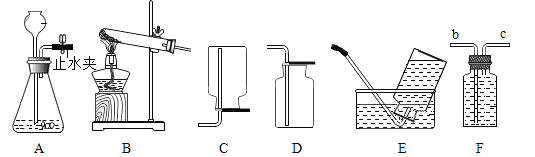
①检查A装置气密性的方法是夹紧止水夹,_____,则气密性良好。
②实验室用金属锌和稀硫酸可以制取氢气,如果想得到较干燥的氢气,可选用的一套制取装置为_____,反应的化学方程式为_____。若采用F装置来收集氢气,氢气应从_____通入(选填b或c)。
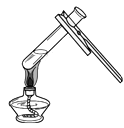
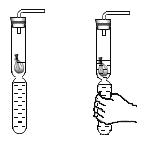
③课外小实验中,小明同学利用废弃的“棒棒冰”塑料为材料制成了如图所示的气体发生装置。该装置与A装置相比的优点有哪些_____(写出一点即可)
(4)某兴趣小组利用废铁屑与废硫酸起反应来制取硫酸亚铁(只考虑铁与酸的反应)他们将6g废铁屑放入烧杯中,缓慢加入废硫酸直至不再产生气泡。发现加入废硫酸的质量为98g,最后称得称量烧杯的总质量为103.8g(不含烧杯的质量)。试求制取硫酸亚铁的质量为多少_____?