题目内容
水是生命之源,与生活生产关系密切.保护水环境、珍爱水资源,是每个公民应尽的责任和义务.
(1)为了防止水的污染,下列做法有利于保护水资源的是
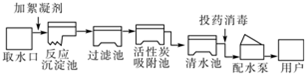
天然水中含有许多杂质,自来水生产过程中,常用过滤的方法除去水中悬浮的杂质,同时还必须进行消毒.ClO2是一种新型的自来水消毒剂,工业上用Cl2与NaClO2制取ClO2.请配平下列化学方程式:
(2)在化学实验和科学研究中,水也是一种常用的试剂.水分子在特定条件下容易得到一个H+,形成水合氢离子(H3O+).下列对上述过程的描述不合理的是
A.氧元素发生了改变 B.微粒的组成发生了改变
C.微粒的化学性质发生了改变 D.与水分子比水合离子的电子数发生了改变
研究人员最近发现,在一定的实验条件下,给水施加一个弱电场,在常温、常压下,水可以结成冰,称为“热冰”.“热冰”有许多实用价值,如开发新药、用于纳米打印机等,还可能用来
A.代替干冰 B.防止冰川熔化 C.在室温下制作冰雕 D.建室温溜冰场
(3)医药上可用石膏来固定骨折部位.石膏有熟石膏(CaSO4?
H2O,一种白色粉末)和生石膏(CaSO4?2H2O,一种坚硬的固体)两种,固定骨折的石膏是
(1)为了防止水的污染,下列做法有利于保护水资源的是
②④
②④
(填编号).①抑制水中所有动、植物的生长;②不任意排放工业废水;③大量使用化肥农药;④生活污水经过净化处理后再排放.天然水中含有许多杂质,自来水生产过程中,常用过滤的方法除去水中悬浮的杂质,同时还必须进行消毒.ClO2是一种新型的自来水消毒剂,工业上用Cl2与NaClO2制取ClO2.请配平下列化学方程式:
1
1
Cl2+2
2
NaClO2═2NaCl+2
2
ClO2(2)在化学实验和科学研究中,水也是一种常用的试剂.水分子在特定条件下容易得到一个H+,形成水合氢离子(H3O+).下列对上述过程的描述不合理的是
A D
A D
(填序号).A.氧元素发生了改变 B.微粒的组成发生了改变
C.微粒的化学性质发生了改变 D.与水分子比水合离子的电子数发生了改变
研究人员最近发现,在一定的实验条件下,给水施加一个弱电场,在常温、常压下,水可以结成冰,称为“热冰”.“热冰”有许多实用价值,如开发新药、用于纳米打印机等,还可能用来
C D
C D
(填写序号)A.代替干冰 B.防止冰川熔化 C.在室温下制作冰雕 D.建室温溜冰场
(3)医药上可用石膏来固定骨折部位.石膏有熟石膏(CaSO4?
| 1 |
| 2 |
CaSO4?
H2O(或2CaSO4?H2O)
| 1 |
| 2 |
CaSO4?
H2O(或2CaSO4?H2O)
(填化学式).固定时发生反应的化学方程式| 1 |
| 2 |
2CaSO4?
H2O+3H2O=2CaSO4?2H2O
| 1 |
| 2 |
2CaSO4?
H2O+3H2O=2CaSO4?2H2O
.| 1 |
| 2 |
分析:(1)可以根据合理利用水资源和防止环境污染方面进行分析、判断,从而得出正确的结论;根据化学反应前后原子的种类和数量不变进行配平;
(2)根据H+和水结合形成水合氢离子的实质来分析;
根据题意信息:水施加一个弱电场后,在常温、常压下,水可以结成冰,即为“热冰”,可知热冰溶解过程会吸热,具有冰的物理性质等;
(3)根据生石膏和熟石膏的性质区别以及二者之间的相互转化关系来回答.
(2)根据H+和水结合形成水合氢离子的实质来分析;
根据题意信息:水施加一个弱电场后,在常温、常压下,水可以结成冰,即为“热冰”,可知热冰溶解过程会吸热,具有冰的物理性质等;
(3)根据生石膏和熟石膏的性质区别以及二者之间的相互转化关系来回答.
解答:解:(1)保护水资源的措施即不会导致水污染的做法,大量使用化肥农药不利于保护水资源,抑制水中所有动、植物的生长会使水质变坏,从而使水受污染,故选②④;根据化学反应前后原子的种类和数量不变的原则,利用观察法可以对化学方程式进行配平,其系数应分别为:1、2、2;
(2)H+和水结合形成水合氢离子的方程式为:H++H2O=H3O+,根据质量守恒定律可知,元素种类没有变化,元素化合价也没有变化,微粒组成由分子和离子结合成为离子而发生变化,化学性质也变为酸性,但过程前后电子总数均为10电子,无变化,故选:A、D;
根据热冰的概念和形成条件可知,热冰实质仍然是水,故不能做代替干冰和防止冰川熔化等用途;根据热冰的特点“在常温、常压下,水可以结成冰”可知在室温下可以制作冰雕,还能建室温溜冰场.故答案为:C、D.
(3)医药上可用熟石膏来固定骨折部位,熟石膏在一定的温度下和水结合变为较大硬度的生石膏,从而起到固定作用,方程式为:2(CaSO4?
H2O)+3H2O=2(CaSO4?2H2O).
故答案为:(1)②④;1、2、2;(2)AD;CD;(3)CaSO4?
H2O(或2CaSO4?H2O);2(CaSO4?
H2O)+3H2O=2(CaSO4?2H2O)
(2)H+和水结合形成水合氢离子的方程式为:H++H2O=H3O+,根据质量守恒定律可知,元素种类没有变化,元素化合价也没有变化,微粒组成由分子和离子结合成为离子而发生变化,化学性质也变为酸性,但过程前后电子总数均为10电子,无变化,故选:A、D;
根据热冰的概念和形成条件可知,热冰实质仍然是水,故不能做代替干冰和防止冰川熔化等用途;根据热冰的特点“在常温、常压下,水可以结成冰”可知在室温下可以制作冰雕,还能建室温溜冰场.故答案为:C、D.
(3)医药上可用熟石膏来固定骨折部位,熟石膏在一定的温度下和水结合变为较大硬度的生石膏,从而起到固定作用,方程式为:2(CaSO4?
| 1 |
| 2 |
故答案为:(1)②④;1、2、2;(2)AD;CD;(3)CaSO4?
| 1 |
| 2 |
| 1 |
| 2 |
点评:本题是一道综合性很强的题目,要求学生从各个角度掌握基本知识,难度较大.本题围绕“水”做为主题设置情景,既将环境保护与化学知识联系起来,突出了化学STSE试题的主旨,又起到了宣传知识,体现生产生活,提高学生实际应用知识能力.问题并不难,可要求学生考虑全面并不容易,特别针对“热冰”这个新的概念,要牢牢抓住实质仍然是水,故不能做代替干冰和防止冰川熔化等用途.

练习册系列答案
相关题目
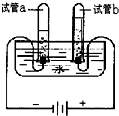 水是人类最宝贵的自然资源.没有水就没有生命,根据你所掌握的有关水的知识回答下列问题:
水是人类最宝贵的自然资源.没有水就没有生命,根据你所掌握的有关水的知识回答下列问题: