题目内容
水是一种重要的物质,在实验室和日常生活中有着十分重要的作用.请根据下列提示简要回答相关问题: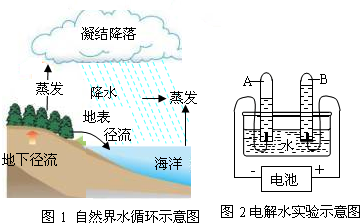
(1)根据图1和图2回答下列问题.
①分析图1可知,在水蒸发的过程中,下列说法正确的是(填字母序号)
A.水分子不断运动 B.水分子之间间隔不变
C.氢、氧原子不发生改变 D.水分子可以保持水的物理性质
②图2的试管A中的气体的化学式是
(2)硬水会给生产和生活带来许多不便,生活中可用
(3)农业和园林浇灌植物时,将大水漫灌改为喷灌、滴灌的目的是
(4)生活离不开水,净化水的知识在日常生活中有着广泛的应用.
①用纱网可将茶叶与茶水分离,便于饮用,其应用的分离方法在化学上称为
②自来水厂用二氧化氯消毒杀菌,二氧化氯的化学式为
③自来水厂主要通过 ①吸附沉淀(用明矾) ②投药消毒(用漂白粉等) ③静置沉淀 ④过滤等对自然水进行净化,其合理的步骤顺序是
(5)实验室有一瓶质量分数为36%的浓盐酸,现要配制200g7.3%的稀盐酸,实验步骤有
(6)用该稀盐酸100g和6g含杂质的铁粉完全反应,得到溶液的溶质质量分数是多少?(杂质不和盐酸反应,也不溶于水) (计算结果保留一位小数)
分析:(1)①水蒸发属于物理变化,水分子不变,分子间隔发生变化;②根据电解水的现象和结论回答;
(2)由于硬水中含有较多钙、镁离子,加热煮沸会钙、镁离子会形成不溶于水的水垢而降低含量;
(3)根据将大水漫灌改为喷灌、滴灌浇灌植物,可减小农业用水量,推断其目的;
(4)①根据过滤的原理分析;②根据物质的名称写出化学式;③根据净水的步骤分析解答;
(5)用浓溶液陪着稀溶液的步骤是计算,量取和稀释;
(6)根据铁和盐酸反应的化学方程式,根据盐酸中溶质的质量计算出氯化亚铁,然后根据质量守恒定律计算溶液的质量,再根据溶质质量分数的公式计算生成的溶液的溶质质量分数.
(2)由于硬水中含有较多钙、镁离子,加热煮沸会钙、镁离子会形成不溶于水的水垢而降低含量;
(3)根据将大水漫灌改为喷灌、滴灌浇灌植物,可减小农业用水量,推断其目的;
(4)①根据过滤的原理分析;②根据物质的名称写出化学式;③根据净水的步骤分析解答;
(5)用浓溶液陪着稀溶液的步骤是计算,量取和稀释;
(6)根据铁和盐酸反应的化学方程式,根据盐酸中溶质的质量计算出氯化亚铁,然后根据质量守恒定律计算溶液的质量,再根据溶质质量分数的公式计算生成的溶液的溶质质量分数.
解答:解:(1)①水蒸发的过程中,水分子不断运动,水分子不发生改变,分子中的氢氧原子不变,分子间隔变大,水的状态发生改变,物理性质发生了变化,故选AC;
②电解水时,生成较多的气体是氢气,检验氧气的方法是用带火星的木条,电解水的化学方程式为:2H2O
2H2↑+O2↑;
(2)对水加热煮沸时,可使水中钙、镁离子形成沉淀,因此生活中降低水的硬度的方法是煮沸;
(3)农业和园林浇灌植物时,将大水漫灌改为喷灌、滴灌,可减小农业用水量,主要是为了节约用水;
(4)①用纱网可将茶叶与茶水分离,便于饮用,其应用的分离方法在化学上称为过滤.②自来水厂用二氧化氯消毒杀菌,二氧化氯的化学式为 ClO2,③对自然水进行净化的合理步骤是先静置沉淀大的颗粒,再吸附沉淀小的杂质,然后过滤,最后投药消毒;
(5)用36%的浓盐酸配制200g7.3%的稀盐酸的实验步骤有计算、量取、稀释装瓶、贴标签;
(6)设生成氯化亚铁的质量为x,生成氢气的质量为y,参加反应的铁的质量为z
Fe+2HCl═FeCl2+H2↑
56 73 127 2
z 100g×7.3% x y
=
=
=
x=12.7g y=0.2g z=5.6g
得到溶液的溶质质量分数=
×100%=12.0%
答:得到溶液的溶质质量分数为12.0%.
故答案为:(1)①AC ②H2,带火星的木条复燃;2H2O
2H2↑+O2↑;
(2)煮沸或蒸馏
(3)节约用水
(4)①过滤 ②ClO2 ③3142
(5)计算、量取、稀释
(6)12.0%
②电解水时,生成较多的气体是氢气,检验氧气的方法是用带火星的木条,电解水的化学方程式为:2H2O
| ||
(2)对水加热煮沸时,可使水中钙、镁离子形成沉淀,因此生活中降低水的硬度的方法是煮沸;
(3)农业和园林浇灌植物时,将大水漫灌改为喷灌、滴灌,可减小农业用水量,主要是为了节约用水;
(4)①用纱网可将茶叶与茶水分离,便于饮用,其应用的分离方法在化学上称为过滤.②自来水厂用二氧化氯消毒杀菌,二氧化氯的化学式为 ClO2,③对自然水进行净化的合理步骤是先静置沉淀大的颗粒,再吸附沉淀小的杂质,然后过滤,最后投药消毒;
(5)用36%的浓盐酸配制200g7.3%的稀盐酸的实验步骤有计算、量取、稀释装瓶、贴标签;
(6)设生成氯化亚铁的质量为x,生成氢气的质量为y,参加反应的铁的质量为z
Fe+2HCl═FeCl2+H2↑
56 73 127 2
z 100g×7.3% x y
| 56 |
| z |
| 73 |
| 100g×7.3% |
| 127 |
| x |
| 2 |
| y |
x=12.7g y=0.2g z=5.6g
得到溶液的溶质质量分数=
| 12.7g |
| 100g+5.6g-0.2g |
答:得到溶液的溶质质量分数为12.0%.
故答案为:(1)①AC ②H2,带火星的木条复燃;2H2O
| ||
(2)煮沸或蒸馏
(3)节约用水
(4)①过滤 ②ClO2 ③3142
(5)计算、量取、稀释
(6)12.0%
点评:本题考查了水的净化方法,同时涉及化学方程的书写和计算,要能灵活应用课本所知识,并做认真分析,在根据化学方程式进行计算时要注意步骤和结果的准确性.

练习册系列答案
相关题目
 (2012?洛江区质检)化学是人类进步的阶梯,学习化学知识后,观察物质世界就要从化学视角看.水是一种重要的物质,在日常生活和实验室中有着不可替代的作用.请按要求回答下列问题:
(2012?洛江区质检)化学是人类进步的阶梯,学习化学知识后,观察物质世界就要从化学视角看.水是一种重要的物质,在日常生活和实验室中有着不可替代的作用.请按要求回答下列问题: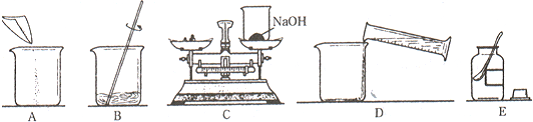
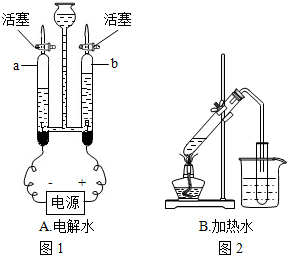 学习化学知识后,物质世界可用化学视角观察了.水是一种重要的物质,在日常生活和实验室中有着不可替代的作用.
学习化学知识后,物质世界可用化学视角观察了.水是一种重要的物质,在日常生活和实验室中有着不可替代的作用.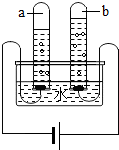 学习化学知识后,观察物质世界就要从化学视角看.水是一种重要的物质,在日常生活和实验室中有着不可替代的作用.请按要求回答下列问题:
学习化学知识后,观察物质世界就要从化学视角看.水是一种重要的物质,在日常生活和实验室中有着不可替代的作用.请按要求回答下列问题: