题目内容
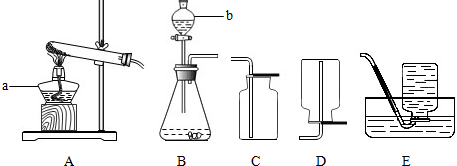
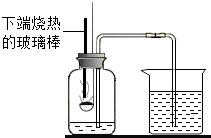
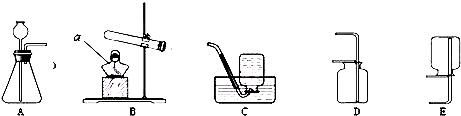
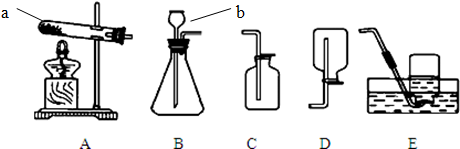
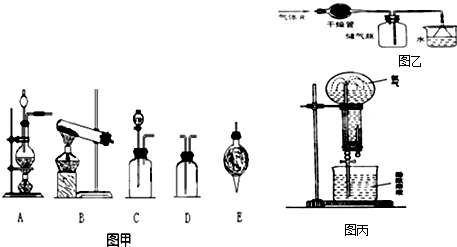
如图回答问题(1)装置A中试管口稍向下倾斜的原因:______.
(2)使用装置B时,长颈漏斗的下端口一定要浸入液面下,目的是______.
(3)采用装置C或E时,导管要插到集气瓶底部,目的是______.
(4)用加热固体甲和固体乙的混合物来制取气体丙,应选用的发生装置是______;若收集丙时只能用E装置,则可推知气体丙性质可能有______、______.
(5)分别写出实验室用B、C组合和B、D组合制取两种不同气体的化学反应方程式(各写一个)
①______.
②______ 2H2O+O2↑
【答案】分析:根据常见气体的制取装置和收集装置的注意事项分析操作;根据气体发生装置的选择依据反应物的状态和反应条件,气体的收集方法依据气体的密度和溶解性分析;根据制取气体选择发生装置的特点是固液在常温下的反应选择气体的制取;根据气体的密度和水溶性分析气体的收集方法,综合分析写出合适的气体制取方程式.
解答:解;(1)装置A中试管口稍向下倾斜的原因:防止冷凝水倒流使试管炸裂;
故答案为:防止冷凝水倒流使试管炸裂;
(2)使用装置B时,长颈漏斗的下端口一定要浸入液面下,目的是:防止生成的气体从长颈漏斗口溢出;
故答案为:防止生成的气体从长颈漏斗口溢出;
(3)采用排空气法收集气体时,导管要插到集气瓶底部,目的是:排尽装置内的空气,收集到较纯净的气体;
故答案为:排尽装置内的空气,收集到较纯净的气体;
(4)用加热固体甲和固体乙的混合物来制取气体丙,发生装置属于固体加热型的A装置;若收集丙时只能用E装置-向下排空气法,则可推知气体丙性质可能有:易溶于水、密度比空气小;
故答案为:A;易溶于水、密度比空气小;
(5)用石灰石和稀盐酸来制取二氧化碳,不需要加热,可以选择的发生装置是B,二氧化碳的密度比空气的密度大,能溶于水,因此只能用向上排空气法收集,因此可以采用B、C组合,反应的方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;用过氧化氢溶液和二氧化锰制取氧气,不需要加热,可以选择的发生装置是B,氧气的密度比空气大,不易溶于水,因此可以采用向上排空气法或排水法收集,因此可以采用B、C或B、D组合,反应的方程式为:2H2O2 2H2O+O2↑.
2H2O+O2↑.
故答案为:CaCO3+2HCl=CaCl2+H2O+CO2↑;2H2O2 2H2O+O2↑.
2H2O+O2↑.
点评:本题考查了常见气体的制取装置、收集方法的选择依据及装置的注意事项的分析,难度不大,关键是明确气体发生装置的选择依据反应物的状态和反应条件,气体的收集方法依据气体的密度和溶解性.
解答:解;(1)装置A中试管口稍向下倾斜的原因:防止冷凝水倒流使试管炸裂;
故答案为:防止冷凝水倒流使试管炸裂;
(2)使用装置B时,长颈漏斗的下端口一定要浸入液面下,目的是:防止生成的气体从长颈漏斗口溢出;
故答案为:防止生成的气体从长颈漏斗口溢出;
(3)采用排空气法收集气体时,导管要插到集气瓶底部,目的是:排尽装置内的空气,收集到较纯净的气体;
故答案为:排尽装置内的空气,收集到较纯净的气体;
(4)用加热固体甲和固体乙的混合物来制取气体丙,发生装置属于固体加热型的A装置;若收集丙时只能用E装置-向下排空气法,则可推知气体丙性质可能有:易溶于水、密度比空气小;
故答案为:A;易溶于水、密度比空气小;
(5)用石灰石和稀盐酸来制取二氧化碳,不需要加热,可以选择的发生装置是B,二氧化碳的密度比空气的密度大,能溶于水,因此只能用向上排空气法收集,因此可以采用B、C组合,反应的方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;用过氧化氢溶液和二氧化锰制取氧气,不需要加热,可以选择的发生装置是B,氧气的密度比空气大,不易溶于水,因此可以采用向上排空气法或排水法收集,因此可以采用B、C或B、D组合,反应的方程式为:2H2O2
 2H2O+O2↑.
2H2O+O2↑.故答案为:CaCO3+2HCl=CaCl2+H2O+CO2↑;2H2O2
 2H2O+O2↑.
2H2O+O2↑.点评:本题考查了常见气体的制取装置、收集方法的选择依据及装置的注意事项的分析,难度不大,关键是明确气体发生装置的选择依据反应物的状态和反应条件,气体的收集方法依据气体的密度和溶解性.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目