��Ŀ����
����Ŀ����ѧС��ͬѧ�ڿ�������п�������ͨ��CO2��������������Щ����(��Na)�Ż𣬲�����CO2Ϩ�𡣡����Ǿ���̽��CO2��Na��Ӧ�IJ��
��������롿CO2��Na��Ӧ��������4�����ʣ�C��CO��Na2O��Na2CO3��
���������ϡ�
��Na�Ƿdz����õĽ�������������O2��H2O�����ʷ�Ӧ��
�ڼ��Ե�Na2CO3��Һ�����Ե�CaCl2��Һ�������ֽⷴӦ��
��Na2O�ǰ�ɫ���壬��H2O��Ӧ����NaOH��
�����Ȼ���(PdCl2)��Һ��ͨ��CO��������ɫ������
��ʵ����̡�ͬѧ������ʦ��ָ�������������ͼ��ʾװ��(���ּг���������ȥ)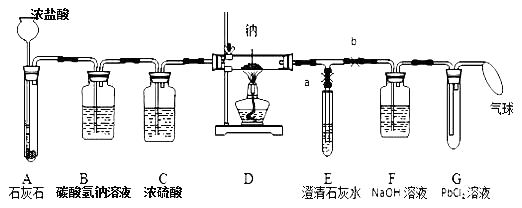
��1��ʵ���¼
��� | ʵ����� | ��Ҫʵ������ | ʵ����ۺͽ��� |
�� | ��a���ر�b���ɳ���©��ע��Ũ���� | A�в�����������E�г��ֻ��� | E�з�Ӧ�Ļ�ѧ����ʽΪ |
�� | ��E�г��ֻ���ʱ����b���ر�a����ȼ�ƾ��� | D��Na����ȼ�գ����������ڱڸ��ź�ɫ����ɫ����G�в�����ɫ���� | ��Ӧ����һ������ |
�� | ȡD�а�ɫ�������Թ��У���ˮ�ܽ⣬�ټ���ʯ��ˮ | ������ɫ���� | ��Ӧ���ﻹ�� |
��2��ʵ�鷴˼
��ʵ���¼���У�E�г��ֻ��ǣ��ٵ�ȼ�ƾ��Ƶ�Ŀ����
��װ��B�з����ķ�Ӧ�Ļ�ѧ����ʽ�� �� ����װ��C����ʵ����Ӱ�����������
�ۼ����4�ַ�Ӧ�����Ƿ���ڵ�ʵ�鷽����ȡD�а�ɫ�������Թ��У���ˮ�ܽ⣬��
��3�����ݷ���������ʵ�������������Ҫ8.8g������̼�μӷ�Ӧ����������Ҫ������20%��ʯ��ʯ�������Ƕ��٣���д��������̣�
���𰸡�
��1��CO2+Ca(OH)2=CaCO3��+H2O,C,CO,Na2CO3
��2���ų�װ���еĿ���,��ֹ�����ĸ���,NaHCO3+HCl=NaCl+H2O+CO2��,ˮ,�������CaCl2��Һ�����ٲ�������,���ϲ���Һ�еμӷ�̪��Һ,��Һ�ʺ�ɫ��˵�� ɫ�����к�Na2O;����Һ����ɫ,�������û��Na2O
��3���⣺����Ҫʯ��ʯ������ΪX
CaCO3 | CO2�� |
100 | 44 |
X��1-20%�� | 8.8g |
![]()
X=25g
����Ҫʯ��ʯ������Ϊ25g
����������1�����������ƺͶ�����̼��Ӧ�Ļ�ѧ����ʽΪ��Ca��OH��2+CO2�TCaCO3��+H2O�����ڱڸ��ź�ɫ���壬˵����Ӧ������̼��G�в�����ɫ������˵����Ӧ������һ����̼ ��ȡD�а�ɫ�������Թ��У���ˮ�ܽ⣬�ټ���ʯ��ˮ��������ɫ������˵����Ӧ���ﻹ��Na2CO3(2) ��ʵ���¼���У�E�г��ֻ��ǣ��ٵ�ȼ�ƾ��Ƶ�Ŀ���Ƿ�ֹ�����е�������ˮ��ʵ��������ţ���Ũ����ӷ��Ȼ���������̼�����Ʒ�ӦNaHCO3+HCl=NaCl+H2O+CO2����Cװ����Ũ����������ã��ʶ�ʵ����Ӱ���������ˮ���ۼ������CaCl2��Һ�����ٲ������������ϲ���Һ�еμӷ�̪��Һ����Һ�ʺ�ɫ��˵�� ɫ�����к�Na2O;����Һ����ɫ���������û��Na2O��
���Դ��ǣ�CO2+Ca(OH)2=CaCO3��+H2O;C;CO;Na2CO3;�ų�װ���еĿ�������ֹ�����ĸ���;NaHCO3+HCl=NaCl+H2O+CO2��;ˮ;�������CaCl2��Һ�����ٲ������������ϲ���Һ�еμӷ�̪��Һ����Һ�ʺ�ɫ��˵�� ɫ�����к�Na2O;����Һ����ɫ���������û��Na2O;
�⣺����Ҫʯ��ʯ������ΪX
CaCO3 | CO2�� |
100 | 44 |
X��1-20%�� | 8.8g |
![]()
X=25g
����Ҫʯ��ʯ������Ϊ25g��
�����㾫�������ն�����̼�Ļ�ѧ�����ǽ����ĸ�������Ҫ֪����ѧ���ʣ�һ������²���ȼ��,Ҳ��֧��ȼ�գ����ܹ�����������ˮ��Ӧ����̼���ʹ�����ʯ��ˮ����ǣ������ȵ�̼��Ӧ��