题目内容
【题目】(5分)工业上制备K2SO4晶体的工艺流程图如下。
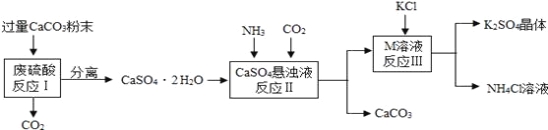
请根据流程回答问题:
(1)将CaCO3研成粉末的目的是 。
(2)写出反应Ⅰ中的化学方程式__________________ ________。
(3)上述流程中可循环使用的物质有CaCO3和 (填化学式)。
(4)不用水而用饱和K2SO4溶液洗涤反应Ⅲ所得晶体的原因是 。为检验硫酸钾晶体是否洗涤干净,可取最后一次洗涤液,先加入______(填序号),振荡、静置,再向上层清液中滴加AgNO3溶液 ,观察现象即可判断。
a.过量的BaCl2溶液 b.过量的Ba(NO3)2溶液
【答案】(1)增大接触面积,加快反应速率(或使反应充分进行或提高原料的利用率)
(2)CaCO3+ H2SO4== CaSO4+H2O+CO2↑
(3)CO2
(4)防止硫酸钾晶体溶于水,减少损耗; b
【解析】
试题分析:(1)将CaCO3研成粉末可以增大接触面积,加快反应速率;
(2)硫酸与碳酸钙反应生成硫酸钙、水、二氧化碳,其反应的方程式为CaCO3+ H2SO4== CaSO4+H2O+CO2↑;
(3)根据图示可知反应Ⅰ中生成二氧化碳,应Ⅱ中生成的碳酸钙;
(4)根据平衡移动的原理可知不用水而用饱和K2SO4溶液洗涤反应Ⅲ所得晶体的原因是防止硫酸钾晶体溶于水,减少损耗;为了不影响氯离子的检验,检验硫酸钾晶体的可选用过量的硝酸钡溶液使之出现明显的现象。

【题目】比较与分析归纳会使你的头脑变得更职明。请分析下表中信息,回答有关问题:
名称 | 符号 | 原子结构示意图 | 单质化学式 | 常温常压下状态 | 单质与氢气反应 |
氟 | F |
| F2 | _________ | 黑暗处爆炸 |
氯 | Cl |
| Cl2 | 气态 | 光照爆炸 |
溴 | Br |
| Br2 | 液态 | 加热反应 |
碘 | I |
| _________ | 固态 | 持续加热缓慢反应 |
(1)请写出上述表中的空格处应补充的内容
(2)试归纳氟、氯、溴、碘对应单质的性质变化规律(答一点即可):_________。已知:Cl2和Br2的化学性质相似,![]() ,其中/span>HClO也是一种酸,试写出Br2与水反应的化学方程式__________。
,其中/span>HClO也是一种酸,试写出Br2与水反应的化学方程式__________。