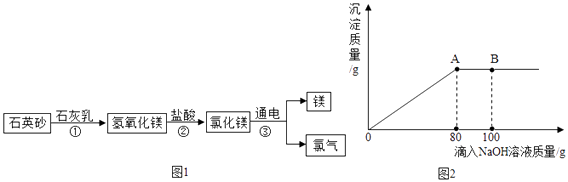
ΧβΡΩΡΎ»ί
ΓΨΧβΡΩΓΩ―θΤχ‘Ύ»’≥Θ…ζΜνΚΆT“Β…ζ≤ζ÷–ΒΡ”ΟΆΨΖ«≥ΘΙψΖΚΘ§Τδ Β―ι “ΒΡ÷Τ»Γ «Μ·―ß―–ΨΩΒΡ÷Ί“ΣΡΎ»ίΓΘ
Θ®1Θ©ΗυΨίœ¬Ν– Β―ιΉΑ÷ΟΆΦΜΊ¥πΈ Χβ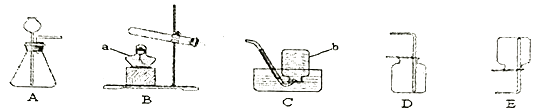
ΔΌ–¥≥ω±ξ”–Ή÷ΡΗΒΡ“«ΤςΟϊ≥ΤΘΚa Θ§b ΓΘ
ΔΎ–¥≥ωAΉΑ÷Ο÷Τ»ΓO2ΒΡΜ·―ßΖΫ≥Χ Ϋ ΓΘ
Δέ»τΉΑ÷ΟD ’Φ·―θΤχΘ§―ι¬ζΒΡΖΫΖ® « ΓΘ
Θ®2Θ© Β―ι “≥Θ”ΟΦ”»»¬»ΥαΦΊ”κΕΰ―θΜ·ΟΧΜλΚœΈοΒΡΖΫΖ®÷Τ»Γ―θΤχΘ§–¥≥ωΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΘΚ ΘΜ
Θ®3Θ©–ΓΖΦΖΔœ÷Θ§¬»ΥαΦΊ”κ―θΜ·Ά≠ΜλΚœΦ”»»Θ§“≤ΡήΫœΩλ≤ζ…ζ―θΤχΘ§”Ύ «Ϋχ––»γœ¬ΧΫΨΩΘΚ
ΓΨΧα≥ω≤¬œκΓΩ≥ΐMnO2 Θ§ CuOΆβΘ§Fe2O3 Θ§ “≤Ω…“‘ΉςKClO3Ζ÷ΫβΒΡ¥ΏΜ·ΦΝΓΘ
ΓΨ Β―ι―ι÷ΛΓΩΑ¥œ¬±μΫχ–– Β―ιΘΚΨ≠≤βΕ®Ζ÷ΫβΈ¬Ε»Θ®Ζ÷ΫβΈ¬Ε»‘ΫΒΆΘ§¥ΏΜ·–ßΙϊ‘ΫΚΟΘ©ΓΘ
Β―ι±ύΚ≈ | Β―ι“©ΤΖ | Ζ÷ΫβΈ¬Ε»( |
ΔΌ | KClO3 | 580 |
ΔΎ | KClO3ΓΔMnO2÷ ΝΩ±»1ΘΚ1Θ© | 350 |
Δέ | KClO3 Θ§ CuOΘ®÷ ΝΩ±»1ΘΚ1Θ© | 370 |
Δή | KClO3ΓΔFe2O3Θ®÷ ΝΩ±»1ΘΚ1Θ© | 390 |
ΓΨΖ÷Έω ΐΨίΓΔΒΟ≥ωΫα¬έΓΩ”… Β―ι”κ Β―ιΔήΕ‘±»Θ§÷ΛΟς≤¬œκΚœάμΓΘ
Θ®4Θ©ΓΨΆΊ’Ι―”…λΓΩ»γΙϊΫΪKMnO4ΙΧΧε”κKClO3ΙΧΧεΜλΚœΦ”»»Θ§‘ρKClO3ΒΡΖ÷ΫβΥΌ¬ ¥σ¥σΦ”ΩλΓΘ«κΥΒΟςKMnO4‘ΎKClO3ΒΡΖ÷ΫβΖ¥”Π÷– «ΖώΉς¥ΏΜ·ΦΝΘ§ΈΣ ≤Ο¥ΘΩ
Θ®5Θ©ΓΨ Β―ιΖ¥ΥΦΓΩΆ§÷÷¥ΏΜ·ΦΝΘ§Ω≈ΝΘ¥σ–ΓΩ…Ρή”Αœλ¥ΏΜ·–ßΙϊΘ§«κ…ηΦΤ Β―ιΖΫΑΗΫχ––―ι÷Λ ΓΘ
Θ®6Θ©‘Ύ Β―ι “÷–”ΟΗΏΟΧΥαΦΊ÷Τ»Γ―θΤχΘ§»τ≤ζ…ζ9.6ΩΥ―θΤχ–η“ΣΖ÷ΫβΩΥΗΏΟΧΥαΦΊΘΩ
ΓΨ¥πΑΗΓΩ
Θ®1Θ©ΨΤΨΪΒΤ,Φ·ΤχΤΩ,2H2O2 ![]() 2H2O+ O2Γϋ,ΫΪ¥χΜπ–«ΒΡΡΨΧθΖ≈‘ΎΦ·ΤχΤΩΩΎ,»τΡΨΧθΗ¥»Φ,ΥΒΟς―θΤχ“―Ψ≠ ’Φ·¬ζΝΥ
2H2O+ O2Γϋ,ΫΪ¥χΜπ–«ΒΡΡΨΧθΖ≈‘ΎΦ·ΤχΤΩΩΎ,»τΡΨΧθΗ¥»Φ,ΥΒΟς―θΤχ“―Ψ≠ ’Φ·¬ζΝΥ
Θ®2Θ©2KClO3 ![]() 2KCl+3O2 Γϋ
2KCl+3O2 Γϋ
Θ®3Θ©ΔΌ
Θ®4Θ©ΗΏΟΧΥαΦΊ≤Μ «¥ΏΜ·ΦΝ, «“ρΈΣΦ”ΝΥΗΏΟΧΥαΦΊ÷°Κσ,≤ζ…ζ―θΤχΥΌΕ»Φ”Ωλ «“ρΈΣΗΏΟΧΥαΦΊΖ÷Ϋβ“≤Μα≤ζ…ζ―θΤχ,Ά§ ±≤ζ…ζΒΡΕΰ―θΜ·ΟΧΕ‘¬»ΥαΦΊΒΡΖ÷ΫβΤπ¥ΏΜ·Ής”Ο
Θ®5Θ©ΫΪ¬»ΥαΦΊ”κ≤ΜΆ§Ω≈ΝΘ¥σ–ΓΒΡΆ§÷÷¥ΏΜ·ΦΝΒ»±»≥δΖ÷ΜλΚœ,Φ”»»,≤βΕ®Ζ÷ΫβΈ¬Ε»Θ®ΤδΥϊΚœάμΫβ¥πΨυΗχΖ÷Θ©
Θ®6Θ©9.6
ΓΨΫβΈωΓΩΘ®1Θ©ΔΌΗυΨίΆΦ ΨΘ§“«ΤςΟϊ≥ΤΘΚa «ΨΤΨΪΒΤΘ§b «Φ·ΤχΤΩΘΜΔΎAΉΑ÷Ο ”Ο”ΎΙΧΧεΚΆ“ΚΧε≥ΘΈ¬Ζ¥”Π÷Τ»ΓΤχΧεΘ§Μ·―ßΖΫ≥Χ ΫΈΣΘΚ2H2O2 ![]() 2H2O + O2ΓϋΘΜΔέ»τ”Οœρ…œ≈≈Ω’ΤχΖ® ’Φ·―θΤχ ±Θ§–η―ι¬ζΘ§ΖΫΖ® «ΘΚΫΪ¥χΜπ–«ΒΡΡΨΧθ…λ»κΒΫΤΩΩΎ¥ΠΘ§»τΡΨΧθΗ¥»ΦΘ§‘ρ÷ΛΟς ’Φ·¬ζΝΥΘΜ
2H2O + O2ΓϋΘΜΔέ»τ”Οœρ…œ≈≈Ω’ΤχΖ® ’Φ·―θΤχ ±Θ§–η―ι¬ζΘ§ΖΫΖ® «ΘΚΫΪ¥χΜπ–«ΒΡΡΨΧθ…λ»κΒΫΤΩΩΎ¥ΠΘ§»τΡΨΧθΗ¥»ΦΘ§‘ρ÷ΛΟς ’Φ·¬ζΝΥΘΜ
Θ®2Θ©Φ”»»¬»ΥαΦΊ”κΕΰ―θΜ·ΟΧΜλΚœΈοΒΡΜ·―ßΖΫ≥Χ ΫΘΚ2KClO3 ![]() 2KCl+3O2 ΓϋΘΜ
2KCl+3O2 ΓϋΘΜ
Θ®3Θ©ΓΨΖ÷Έω ΐΨίΓΔΒΟ≥ωΫα¬έΓΩΗυΨί¥ΏΜ·ΦΝΡήΗΡ±δΜ·―ßΖ¥”ΠΒΡΥΌ¬ Θ§Ω…―Γ‘ώΦ”¥ΏΜ·ΦΝΚΆ≤ΜΦ”¥ΏΜ·ΦΝΒΡΫχ––±»ΫœΖ÷ΫβΈ¬Ε»Φ¥Ω…Θ§“Σœκ÷ΛΟς≥ΐMnO2ΓΔCuOΆβΘ§Fe2O3“≤Ω…“‘ΉςKCl03Ζ÷ΫβΒΡ¥ΏΜ·ΦΝΘ§Ω…―Γ‘ώ Β―ιΔΌΚΆ Β―ιΔήΕ‘±»Θ§÷ΛΟς≤¬œκΚœάμΘΜ
Θ®4Θ©ΓΨΆΊ’Ι―”…λΓΩΦ”»»ΗΏΟΧΥαΦΊΩ…“‘Ζ÷Ϋβ≥…ΟΧΥαΦΊΓΔΕΰ―θΜ·ΟΧΓΔ―θΤχΘ§Εΰ―θΜ·ΟΧΨΆΡήΙΜΕ‘¬»ΥαΦΊΒΡΖ÷ΫβΤπΒΫ¥ΏΜ·ΒΡΉς”ΟΘΜ
Θ®5Θ©ΓΨ Β―ιΖ¥ΥΦΓΩ¥ΏΜ·ΦΝ”κΖ¥”ΠΈοΒΡ÷ ΝΩ±»≤ΜΆ§Θ§¥ΏΜ·–ßΙϊ≤ΜΆ§ΘΜ»ΓΩ≈ΝΘ¥σ–ΓœύΆ§ΒΡΆ§“Μ¥ΏΜ·Φ͔ꬻΥαΦΊ“‘≤ΜΆ§÷ ΝΩ±»≥δΖ÷ΜλΚœΘ§Ζ÷±πΦ”»»Θ§≤βΕ®Ζ÷ΫβΈ¬Ε»ΘΜ
Θ®6Θ©…η≤ζ…ζ9.6ΩΥ―θΤχ–η“ΣΖ÷ΫβΗΏΟΧΥαΦΊΒΡ÷ ΝΩΈΣx,
2KMnO4 | O2 Γϋ |
2ΓΝ158 | 2ΓΝ16 |
x | 9.6g |
![]() =
=![]()
![]()
x = 94.8g .
Υυ“‘¥πΑΗ «ΘΚΘ®1Θ©ΨΤΨΪΒΤΘΜΦ·ΤχΤΩΘΜ2H2O2 ![]() 2H2O+ O2ΓϋΘΜΫΪ¥χΜπ–«ΒΡΡΨΧθΖ≈‘ΎΦ·ΤχΤΩΩΎΘ§»τΡΨΧθΗ¥»ΦΘ§ΥΒΟς―θΤχ“―Ψ≠ ’Φ·¬ζΝΥΘΜΘ®2Θ©2KClO3
2H2O+ O2ΓϋΘΜΫΪ¥χΜπ–«ΒΡΡΨΧθΖ≈‘ΎΦ·ΤχΤΩΩΎΘ§»τΡΨΧθΗ¥»ΦΘ§ΥΒΟς―θΤχ“―Ψ≠ ’Φ·¬ζΝΥΘΜΘ®2Θ©2KClO3![]() 2KCl+3O2 ΓϋΘΜΘ®3Θ©ΔΌΘΜΘ®4Θ©ΗΏΟΧΥαΦΊ≤Μ «¥ΏΜ·ΦΝΘ§ «“ρΈΣΦ”ΝΥΗΏΟΧΥαΦΊ÷°ΚσΘ§≤ζ…ζ―θΤχΥΌΕ»Φ”Ωλ «“ρΈΣΗΏΟΧΥαΦΊΖ÷Ϋβ“≤Μα≤ζ…ζ―θΤχΘ§Ά§ ±≤ζ…ζΒΡΕΰ―θΜ·ΟΧΕ‘¬»ΥαΦΊΒΡΖ÷ΫβΤπ¥ΏΜ·Ής”ΟΘΜΘ®5Θ©ΫΪ¬»ΥαΦΊ”κ≤ΜΆ§Ω≈ΝΘ¥σ–ΓΒΡΆ§÷÷¥ΏΜ·ΦΝΒ»±»≥δΖ÷ΜλΚœΘ§Φ”»»Θ§≤βΕ®Ζ÷ΫβΈ¬Ε»Θ®ΤδΥϊΚœάμΫβ¥πΨυΗχΖ÷Θ©ΘΜΘ®6Θ©9.6.
2KCl+3O2 ΓϋΘΜΘ®3Θ©ΔΌΘΜΘ®4Θ©ΗΏΟΧΥαΦΊ≤Μ «¥ΏΜ·ΦΝΘ§ «“ρΈΣΦ”ΝΥΗΏΟΧΥαΦΊ÷°ΚσΘ§≤ζ…ζ―θΤχΥΌΕ»Φ”Ωλ «“ρΈΣΗΏΟΧΥαΦΊΖ÷Ϋβ“≤Μα≤ζ…ζ―θΤχΘ§Ά§ ±≤ζ…ζΒΡΕΰ―θΜ·ΟΧΕ‘¬»ΥαΦΊΒΡΖ÷ΫβΤπ¥ΏΜ·Ής”ΟΘΜΘ®5Θ©ΫΪ¬»ΥαΦΊ”κ≤ΜΆ§Ω≈ΝΘ¥σ–ΓΒΡΆ§÷÷¥ΏΜ·ΦΝΒ»±»≥δΖ÷ΜλΚœΘ§Φ”»»Θ§≤βΕ®Ζ÷ΫβΈ¬Ε»Θ®ΤδΥϊΚœάμΫβ¥πΨυΗχΖ÷Θ©ΘΜΘ®6Θ©9.6.
ΓΨΩΦΒψΨΪΈωΓΩΫβ¥π¥ΥΧβΒΡΙΊΦϋ‘Ύ”ΎάμΫβ―θΤχΒΡ÷Τ»ΓΉΑ÷ΟΒΡœύΙΊ÷Σ ΕΘ§’ΤΈ’ΖΔ…ζΉΑ÷ΟΘΚΙΧΙΧΦ”»»–ΆΓΔΙΧ“Κ≤ΜΦ”»»–ΆΘ§“‘ΦΑΕ‘―θΤχΒΡ ’Φ·ΖΫΖ®ΒΡάμΫβΘ§ΝΥΫβ ’Φ·ΉΑ÷ΟΘΚΗυΨίΈο÷ ΒΡΟήΕ»ΓΔ»ήΫβ–‘ΘΜ≈≈Υ°Ζ® ’Φ· ±Θ§¥ΐΤχ≈ίΨυ‘»Ν§–χΟΑ≥ω ±‘Ό ’Φ·Θ®Η’ΩΣ Φ≈≈≥ωΒΡ « ‘Ιή÷–ΒΡΩ’ΤχΘΜΘ©”Ο≈≈Ω’ΤχΖ® ’Φ·ΤχΧε ±Θ§ΒΦΙή…λΒΫΦ·ΤχΤΩΒΉ≤ΩΘ°

 ΧλΧλœρ…œ“Μ±ΨΚΟΨμœΒΝ–¥πΑΗ
ΧλΧλœρ…œ“Μ±ΨΚΟΨμœΒΝ–¥πΑΗ –Γ―ß…ζ10Ζ÷÷””Π”ΟΧβœΒΝ–¥πΑΗ
–Γ―ß…ζ10Ζ÷÷””Π”ΟΧβœΒΝ–¥πΑΗ