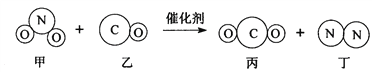
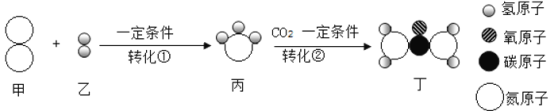
题目内容
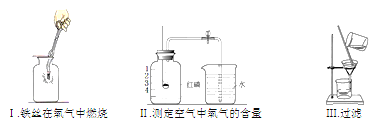
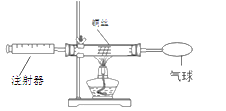
【题目】用如图所示装置进行下列实理验,实验结果与预测的现象不一致的是( )
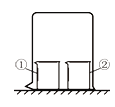
选项 | ①中的物质 | ②中的物质 | 预测①中的现象 |
A | 紫色石蕊试液 | 浓氨水 | 溶液由紫色变为蓝色 |
B | 氢氧化钡溶液 | 浓硫酸 | 有白色沉淀 |
C | 硫酸铜溶液 | 浓氨水 | 有蓝色沉淀 |
D | 硝酸银溶液 | 浓盐酸 | 有白色沉淀 |
A. AB. BC. CD. D
【答案】B
【解析】
A、石蕊遇碱变蓝,氨水显碱性,具有挥发性,故石蕊由紫色变为蓝色,故正确,不符合题意;
B、氢氧化钡和浓硫酸都没有挥发性,故放在两个烧杯中不可能有白色沉淀生成,故错误,符合题意;
C、氨水显碱性,具有挥发性,挥发出来的氨气溶解与硫酸铜溶液中的水中,与硫酸铜反应,生成蓝色的氢氧化铜沉淀,故正确,不符合题意;
D、浓盐酸具有挥发性,挥发出来的氯化氢气体溶解在硝酸银溶液中,与硝酸银反应生成氯化银沉淀,故正确,不符合题意。故选B.

 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案【题目】有一份铜锌合金粉末样品(设只含铜、锌),为认识其组成等,某学习小组进行了以下探究,请参与并完成有关计算:
(1)取样品20g,和足量稀硫酸充分混合,待反应完全后过滤,将滤渣洗涤,干燥后称得其质量为13.5g。该样品中铜的质量分数为______。
(2)再取三份不同质量的样品,分别加入到三份100g相同浓度的硫酸溶液中,充分反应后,测得的数据如下表:
实验序号 | ① | ② | ③ |
样品的质量/g | 10 | 20 | 30 |
生成气体的质量/g | 0.1 | 0.2 | 0.25 |
试计算所用硫酸溶液的溶质质量分数(写出计算过程,结果精确到0.01%)。_______
【题目】2019年为“元素周期表年”,元素周期表是学习和研究化学的重要工具。
(1)原子序数为1~18的元素在元素周期表中的位置如下表所示。
第1周期 | H | He | ||||||
第2周期 | Li | Be | B | C | N | O | F | Ne |
第3周期 | Na | Mg | Al | Si | P | S | Cl | Ar |
①Al属于_____(填“金属”或“非金属”)元素,其原子的核电荷数为______
②Na原子的结构示意图为 ,则钠离子的核外电子数为_______。
,则钠离子的核外电子数为_______。
③周期表中磷元素的有关信息如图所示,图中“30.97”所表示的含义是_______.

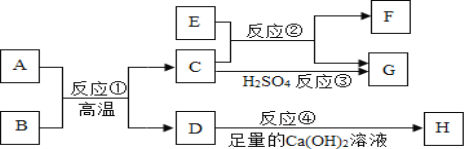
(2)根据周期表体现的结构与性质之间的关系,某同学构建了铜及其化合物的“化合价一物质类别”关系图。
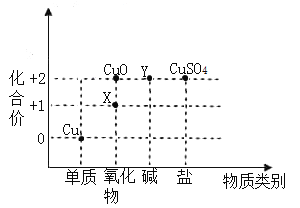
①写出物质X的化学式:_____。
②写出由物质Y转化为![]() 的化学反应方程式:______.
的化学反应方程式:______.
【题目】下表是几种可燃物在常压时的沸点;
可燃物 | CH4 | C2H6 | C3H8 | X | C5H12 |
沸点/℃ | 164 | 88.6 | 42.1 | 0.5 | 36.1 |
(1)在C3H8中,碳元素与氢元素的质量比为_____________(最简整数比)。
(2)在C3H8中,碳元素的质量分数为_____________(计算结果精确至0.1%)。
(3)45gC2H6与_____________gC5H12所含碳元素质量相等。
(4)分析上表中可燃物分子结构上的规律,推测X的化学式为_____________。