题目内容
(9分)某纯碱样品中含有少量氯化钠,现欲测定其中碳酸钠的质量分数,进行如下实验:
《实验原理》:Na2CO3+H2SO4=Na2SO4 + H2O +CO2↑;通过实验测定反应产生的二氧化碳的质量,即可求得原样品中碳酸钠的质量,进而求得碳酸钠在样品中的质量分数。
《实验装置》:如图所示。
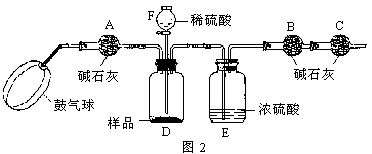
《实验步骤》:①如图连接装置(除B、C外)并加入所需药品。②称量并记录B的质量(m1) (称量时注意封闭B的两端) 。③按动鼓气球,持续约1分钟。④连接上B、C。⑤打开分液漏斗F的活塞,将稀硫酸快速加入D中后,关闭活塞。⑥按动鼓气球,持续约1分钟。⑦称量并记录B的质量(m2)。(称量时注意封闭B的两端及E右端的出口。)⑧计算。请回答:
(1)已知碱石灰的主要成分是氢氧化钙和氢氧化钠,则干燥管A的作用是 ,干燥管C的作用是 ,E装置的作用是 。步骤③中鼓气的目的是 ;步骤⑥中鼓气的目的是 ;本实验能否同时省略③、⑥两个步骤? ,原因是 。
(2)若所取样品的质量为5g,为确保实验顺利进行,分液漏斗F中至少要盛放10%的稀硫酸(密度为1.07g/mL) /mL,若m1为51.20 g ,m2为53.18g ,样品中碳酸钠的质量分数为 。
《实验原理》:Na2CO3+H2SO4=Na2SO4 + H2O +CO2↑;通过实验测定反应产生的二氧化碳的质量,即可求得原样品中碳酸钠的质量,进而求得碳酸钠在样品中的质量分数。
《实验装置》:如图所示。

《实验步骤》:①如图连接装置(除B、C外)并加入所需药品。②称量并记录B的质量(m1) (称量时注意封闭B的两端) 。③按动鼓气球,持续约1分钟。④连接上B、C。⑤打开分液漏斗F的活塞,将稀硫酸快速加入D中后,关闭活塞。⑥按动鼓气球,持续约1分钟。⑦称量并记录B的质量(m2)。(称量时注意封闭B的两端及E右端的出口。)⑧计算。请回答:
(1)已知碱石灰的主要成分是氢氧化钙和氢氧化钠,则干燥管A的作用是 ,干燥管C的作用是 ,E装置的作用是 。步骤③中鼓气的目的是 ;步骤⑥中鼓气的目的是 ;本实验能否同时省略③、⑥两个步骤? ,原因是 。
(2)若所取样品的质量为5g,为确保实验顺利进行,分液漏斗F中至少要盛放10%的稀硫酸(密度为1.07g/mL) /mL,若m1为51.20 g ,m2为53.18g ,样品中碳酸钠的质量分数为 。
(1)除去鼓入空气中的二氧化碳;防止空气中的二氧化碳和水进入B中影响实验结果;防止D中的水蒸气进入B中;用除去二氧化碳的空气赶走体系中的二氧化碳;用除去二氧化碳的空气将反应产生的二氧化碳 全部赶入B中;不能;①空气中含少量二氧化碳、②反应后装置中残留二氧化碳均会造成结论偏差.
(2)43.0;95.4%.
(2)43.0;95.4%.
:(1)干燥管A可以吸收鼓气球中鼓入的空气中的二氧化碳,避免对干燥管B的质量增加造成干扰;干燥管Ⅱ在干燥管I之后,能阻止空气中的二氧化碳和水进入干燥管,E中盛有的是浓硫酸,具有吸水性,能将水分吸除,排除水分对生成二氧化碳质量的影响;步骤③中鼓气的目的是用除去二氧化碳的空气赶走体系中的二氧化碳,步骤⑥鼓入空气是利用压力差使产生的二氧化碳全部被排出,要测定二氧化碳的质量,需排除空气中二氧化碳对生成的二氧化碳的质量的影响;本实验不能同时省略③、⑥两个步骤,否则会给实验带来误差.
(2)当5克样品全部为碳酸钠时,耗硫酸最多,设所需硫酸的质量为x
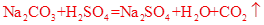
106 98 5 x
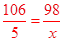 x=4.6(g)
x=4.6(g)
故至少要盛放10%的稀硫酸(密度为1.07g/mL)的体积为:V= ≈43.0(ml)
≈43.0(ml)
根据所测数据,生成二氧化碳的质量为(m2-m1)=1.98g,设碳酸钠的质量为x,则有
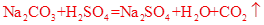
106 44
X 1.98
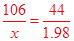
x=4.77(g)
所以纯碱样品纯度为: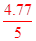 ×100%=95.4%
×100%=95.4%
(2)当5克样品全部为碳酸钠时,耗硫酸最多,设所需硫酸的质量为x
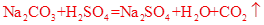
106 98 5 x
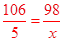 x=4.6(g)
x=4.6(g)故至少要盛放10%的稀硫酸(密度为1.07g/mL)的体积为:V=
 ≈43.0(ml)
≈43.0(ml)根据所测数据,生成二氧化碳的质量为(m2-m1)=1.98g,设碳酸钠的质量为x,则有
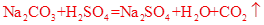
106 44
X 1.98
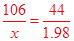
x=4.77(g)
所以纯碱样品纯度为:
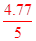 ×100%=95.4%
×100%=95.4%
练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目


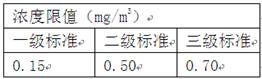
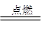 2CO2↑+ 4H2O + 3N2↑ 计算完全燃烧30 t偏二甲肼会产生多少吨水?
2CO2↑+ 4H2O + 3N2↑ 计算完全燃烧30 t偏二甲肼会产生多少吨水?